题目内容
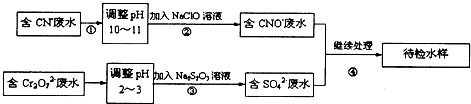
粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳、稀盐酸.
(1)欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为 (只填化学式).
(2)调节pH 的目的 ,试剂b是 (填名称).
(3)洗涤除去NaCl晶体表面附带的少量KCl,选用75%乙醇试剂,使用该试剂的目的是 .
(4)检验产品中是否含有KCl质杂的操作是 .

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳、稀盐酸.
(1)欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为
(2)调节pH 的目的
(3)洗涤除去NaCl晶体表面附带的少量KCl,选用75%乙醇试剂,使用该试剂的目的是
(4)检验产品中是否含有KCl质杂的操作是
考点:粗盐提纯
专题:
分析:(1)把杂质转化为沉淀或气体除去,除钙离子用碳酸根,除镁离子用氢氧根,除硫酸根用钡离子.要注意除杂质的顺序,后加的试剂最好能把前面先加是过量试剂除掉;
(2)加适量盐酸可以除掉过量的OH-、CO32-;
(3)氯化钠晶体中混有氯化钾,必须洗涤,可以根据乙醇的性质来回答;
(4)检验食盐中是否含有KCl,需通过检验K+的存在来确定,而K+的检验需通过焰色反应来确定.
(2)加适量盐酸可以除掉过量的OH-、CO32-;
(3)氯化钠晶体中混有氯化钾,必须洗涤,可以根据乙醇的性质来回答;
(4)检验食盐中是否含有KCl,需通过检验K+的存在来确定,而K+的检验需通过焰色反应来确定.
解答:
解:(1)除去粗盐中的可溶性杂质:Mg2+、Ca2+、SO42-时,可以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,氢氧化钠和氯化钡可以颠倒加入的顺序,
故答案为:BaCl2、NaOH、Na2CO3(或NaOH、BaCl2、Na2CO3或BaCl2、Na2CO3、NaOH);
(2)加适量盐酸,可以少引入杂质,并且盐酸与过量NaOH溶液和过量Na2CO3溶液发生反应,离子方程式为H++OH-═H2O、CO32-+2H+═H2O+CO2↑,从而除掉过量的OH-、CO32-,故答案为:除掉过量的OH-、CO32-;稀盐酸;
(3)粗盐中含有钾离子,所以氯化钠晶体中混有氯化钾,必须进行洗涤,氯化钠不溶于乙醇,可用乙醇冲洗固体表面的氯化钾,这样可以减少晶体的损失,
故答案为:除去晶体表面的KCl,减少晶体的损耗;
(4)检验食盐中是否含有KCl,可以通过K+的检验来确定,而焰色反应的方法是:用洁净的铂丝蘸取待测液放到酒精灯外焰上灼烧,透过蓝色钴玻璃,若火焰呈紫色,则有氯化钾,故答案为:用洁净的铂丝蘸取待测液放到酒精灯外焰上灼烧,透过蓝色钴玻璃,若火焰呈紫色,则有氯化钾.
故答案为:BaCl2、NaOH、Na2CO3(或NaOH、BaCl2、Na2CO3或BaCl2、Na2CO3、NaOH);
(2)加适量盐酸,可以少引入杂质,并且盐酸与过量NaOH溶液和过量Na2CO3溶液发生反应,离子方程式为H++OH-═H2O、CO32-+2H+═H2O+CO2↑,从而除掉过量的OH-、CO32-,故答案为:除掉过量的OH-、CO32-;稀盐酸;
(3)粗盐中含有钾离子,所以氯化钠晶体中混有氯化钾,必须进行洗涤,氯化钠不溶于乙醇,可用乙醇冲洗固体表面的氯化钾,这样可以减少晶体的损失,
故答案为:除去晶体表面的KCl,减少晶体的损耗;
(4)检验食盐中是否含有KCl,可以通过K+的检验来确定,而焰色反应的方法是:用洁净的铂丝蘸取待测液放到酒精灯外焰上灼烧,透过蓝色钴玻璃,若火焰呈紫色,则有氯化钾,故答案为:用洁净的铂丝蘸取待测液放到酒精灯外焰上灼烧,透过蓝色钴玻璃,若火焰呈紫色,则有氯化钾.
点评:本题主要考查了粗盐提纯过程中的除杂方面的知识,综合性强,难度一般,要注意除杂质选取和添加的先后顺序.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
下列各项比较中前者高于(或大于或强于)后者的是( )
| A、金属Mg和金属Cu的空间利用率 |
| B、C-O和Si-O的键能 |
| C、H2SO3和H2SO4中心原子的价层电子对数 |
D、邻羟基苯甲醛(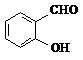 )和对羟基苯甲醛( )和对羟基苯甲醛(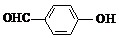 )的沸点 )的沸点 |
某学生只有下列仪器和用具:烧杯、试管、玻璃棒、量筒、托盘天平、胶头滴管、分液漏斗、酒精灯、铁架台、集气瓶、玻璃片、水槽、导管、橡皮塞、橡皮管、药匙、火柴.从缺少仪器或用品的角度看,该学生不能进行的实验操作是( )
| A、制取氢气 |
| B、粗盐提纯 |
| C、分离苯和水的混合物 |
| D、用氯化钠晶体配制100g 5%的氯化钠溶液 |
下列对某些离子的检验及结论一定正确的是( )
| A、加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,则原溶液中一定有SO42- |
| B、加入碳酸钠溶液有白色沉淀生成,再加盐酸,沉淀消失,则原溶液中一定有Ba2+ |
| C、通入Cl2后,溶液变为黄色,加入淀粉后溶液变蓝,则原溶液中一定有I- |
| D、加入NaOH溶液并加热,产生使湿润蓝色石蕊试纸变红的气体,则原溶液一定有NH4+ |
下列说法正确的是( )
| A、从海水中获取物质必须经过化学变化 |
| B、工业上以氯气和澄清石灰水为原料制取漂白粉 |
| C、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” |
| D、氯气泄漏现场应采取喷水雾、喷碱性液体,并杜绝火源、电源等措施 |
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大.X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )
| A、Y与R形成的化合物对应的水化物一定是强酸 |
| B、如W与Y形成化合物的化学式为WY2,则WY2能与碱反应,但不能与任何酸反应 |
| C、原子半径按X、Y、W、R、Z的顺序依次增大 |
| D、R的气态氢化物一定比W的气态氢化物稳定 |