��Ŀ����
�����ֽ�������A��B��C������A����ɫ��ӦΪ��ɫ��B��C�dz������������ֽ�������A��B��C��������ס��ҡ���������D��E��F��G��H֮�䷢������ת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û�б������
�����������Ϣ�ش��������⣺
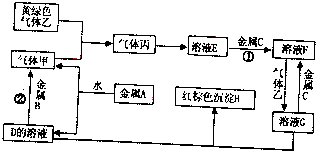
��1��д���������ʵĻ�ѧʽ��B ��G
��2��д�����з�Ӧ�Ļ�ѧ����ʽ���� ����
��3����֤��Ӧ����ҺG�к��н������������õ��Լ��ͷ�Ӧ�Ļ�ѧ����ʽ�� ��
��4����֤��Ӧ����ҺG�в�����ҺF�н��������ӣ���ʵ������
��5������Ӧ����ҺF�н���������ȫ��ת��Ϊ��ҺG�н��������ӣ�ѡ�õ���ɫ�Լ���H2O2��H2O2�����Ե������·���������д����Ӧ�����ӷ���ʽ ��
�����������Ϣ�ش��������⣺

��1��д���������ʵĻ�ѧʽ��B
��2��д�����з�Ӧ�Ļ�ѧ����ʽ����
��3����֤��Ӧ����ҺG�к��н������������õ��Լ��ͷ�Ӧ�Ļ�ѧ����ʽ��
��4����֤��Ӧ����ҺG�в�����ҺF�н��������ӣ���ʵ������
��5������Ӧ����ҺF�н���������ȫ��ת��Ϊ��ҺG�н��������ӣ�ѡ�õ���ɫ�Լ���H2O2��H2O2�����Ե������·���������д����Ӧ�����ӷ���ʽ
���㣺������ƶ�
ר�⣺
������A�ǽ������ʣ�������ɫ��ӦΪ��ɫ����A��Na������ɫ��������Cl2������ɫ������H��Fe��OH��3��Na��ˮ��Ӧ����NaOH��H2�������H2��D��NaOH������B�ܺ�NaOH��Һ��Ӧ������������B��Al��������������Ӧ����HCl�������HCl��E�����ᣬ�����C��Ӧ����F��F�ܺ�������Ӧ����G��G��NaOH��Ӧ����Fe��OH��3����G��FeCl3��F��FeCl2��C��Fe���ٽ����Ŀ�������
���
�⣺A�ǽ������ʣ�������ɫ��ӦΪ��ɫ����A��Na������ɫ��������Cl2������ɫ������H��Fe��OH��3��Na��ˮ��Ӧ����NaOH��H2�������H2��D��NaOH������B�ܺ�NaOH��Һ��Ӧ������������B��Al��������������Ӧ����HCl�������HCl��E�����ᣬ�����C��Ӧ����F��F�ܺ�������Ӧ����G��G��NaOH��Ӧ����Fe��OH��3����G��FeCl3��F��FeCl2��C��Fe��
��1��ͨ�����Ϸ���֪��B��Al��G��FeCl3���ʴ�Ϊ��Al��FeCl3��
��2����Ӧ��Ϊ��������ķ�Ӧ������ʽΪFe+2HCl=FeCl2+H2������Ӧ��ΪAl��NaOH��Һ��Ӧ���ɿ�����ƫ�����ƺ�����������ʽΪ2Al+2NaOH+2H2O�T2NaAlO2+3H2�����ʴ�Ϊ��Fe+2HCl=FeCl2+H2����2Al+2NaOH+2H2O�T2NaAlO2+3H2����
��3��G���������������ӣ�Fe3+��KSCN��Һ��Ӧ����������ʹ��Һ��Ѫ��ɫ����Ӧ����ʽΪFeCl3+3KSCN=Fe��SCN��3+3KCl���ʴ�Ϊ��KSCN��FeCl3+3KSCN=Fe��SCN��3+3KCl��
��4������������ʹ���Ը��������Һ��ɫ��ȡ������ҺG���������Ը��������Һ���۲���������Һ�Ƿ���ɫ���ʴ�Ϊ��ȡ������ҺG���������Ը��������Һ���۲���������Һ�Ƿ���ɫ��
��5��˫��ˮ�Ļ�ԭ������ˮ����Ӧ�����ӷ���ʽ��2Fe2++H2O2+2H+=2Fe3++2H2O���ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O��
��1��ͨ�����Ϸ���֪��B��Al��G��FeCl3���ʴ�Ϊ��Al��FeCl3��
��2����Ӧ��Ϊ��������ķ�Ӧ������ʽΪFe+2HCl=FeCl2+H2������Ӧ��ΪAl��NaOH��Һ��Ӧ���ɿ�����ƫ�����ƺ�����������ʽΪ2Al+2NaOH+2H2O�T2NaAlO2+3H2�����ʴ�Ϊ��Fe+2HCl=FeCl2+H2����2Al+2NaOH+2H2O�T2NaAlO2+3H2����
��3��G���������������ӣ�Fe3+��KSCN��Һ��Ӧ����������ʹ��Һ��Ѫ��ɫ����Ӧ����ʽΪFeCl3+3KSCN=Fe��SCN��3+3KCl���ʴ�Ϊ��KSCN��FeCl3+3KSCN=Fe��SCN��3+3KCl��
��4������������ʹ���Ը��������Һ��ɫ��ȡ������ҺG���������Ը��������Һ���۲���������Һ�Ƿ���ɫ���ʴ�Ϊ��ȡ������ҺG���������Ը��������Һ���۲���������Һ�Ƿ���ɫ��
��5��˫��ˮ�Ļ�ԭ������ˮ����Ӧ�����ӷ���ʽ��2Fe2++H2O2+2H+=2Fe3++2H2O���ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O��
������������Fe��Al���仯����Ϊ���忼���������ƶϣ��������ʵ�������ɫ��״̬���ƶ����ʣ���ȷ���������ǽⱾ��ؼ���������Ľ���Ԫ�ػ����ﻹ��Cu��Na���仯����˽������ӡ��������ӵļ��鷽���������û�ѧ��������ʵ��������Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ
����˵������ȷ���ǣ�������
| A��������ˮ�Ĺ���������ˮ������ķ������� |
| B�����ܵ�Һ��������ķ������� |
| C���������ݵ�����Һ���÷�Һ�ķ������� |
| D��������ˮ��������ˮ�ù��˵ķ������� |
�����Ǿ���ṹ�п��ظ����ֵ���С�Ľṹ��Ԫ��C60�����ṹ��ͼ��ʾ������˵����ȷ���ǣ�������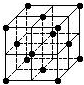

| A��C60�������Ӿ��� |
| B��C60Ħ��������720 |
| C����C60������ƽ��ÿ��������14��C60���� |
| D��ÿ��C60������Χ������������Ⱦ����C60������12�� |
����ʵ���������ȷ���ǣ�������
| A���������ʱ���¶ȼ�ˮ����������ƿ�ĵײ�����������Һ���м��뼸���ʯ���Է�ֹ���� |
| B����������ʱ��Ӧʹ������е�ˮ����ȫ���ɺ���ֹͣ���� |
| C����ɫ��Ӧÿ��ʵ�鶼Ҫ����ϡ����ϴ����˿ |
| D�����ˡ��ᾧ�����ա���ȡ����Һ������ȶ��dz��õķ�������ķ��� |
�����������ᷴӦ��������������ȷ���ǣ�������
| A��������ԭ������������������ |
| B���÷�Ӧ���ڵ��͵ķ��ȷ�Ӧ |
| C������Ѹ÷�Ӧ��Ƴ�ԭ��أ�����п������������ |
| D������£�ת��2mol ���ӣ�������22.4L������ |
����˵�����ʾ��������ȷ���ǣ�������
| A�����������������������ֱ���ȫȼ�գ���Ӧ����ЧӦ��H1����H2 |
| B��NH4HCO3��s���TNH3��g��+H2O��g��+CO2��g����H=+185.57 kJ/mol���Է����У�ԭ������ϵ���Է�������Ҷ����ӵķ���ת������� |
| C����25�桢101 kPaʱ��1��H2��ȫȼ������H2O�ų�����142.9kJ��2H2O��1��=2H2��g��+O2��g����H=-571.6kJ?mol-1 |
| D��ϡ��ǿ���ϡ��ǿ����Һ��Ӧ���Ȼ�ѧ����ʽ��Ϊ��H++OH-=H2O��H=-57.3kJ?mol-1 |
