题目内容
17.常温常压下,将50mL三种气态烃的混合物与足量的氧气混合后点燃爆炸,恢复到原状态时,体积共减少了125mL,则三种烃可能是( )| A. | CH4、C2H2、C3H4 | B. | C2H6、C3H6、C4H6 | C. | C2H6、C3H6、C3H4 | D. | C2H4、C2H6、C3H6 |
分析 常温常压下水为液态,设烃的混合物的平均化学式为CxHy,在氧气中燃烧的化学方程式为CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O(l),根据体积变化利用差量法计算,然后根据计算结果进行判断.
解答 解:设混合烃的平均组成为CxHy,根据完全燃烧通式,则:
CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O(l),△V
1 1+$\frac{y}{4}$
50mL 125mL
则1+$\frac{y}{4}$=$\frac{125mL}{25mL}$=$\frac{5}{2}$,
解得:y=6,
即混合气体分子中平均含有6个H原子,满足条件的只有B,
故选B.
点评 本题考查混合物的有关计算,题目难度中等,注意差量法与平均值法的运用,试题侧重对学生思维能力的考查,有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
7.下列说法不正确的是( )
| A. | 在25℃时,将c mol•L-1的醋酸溶液与0.02mol•L-1NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=$\frac{2×{10}^{-9}}{c-0.02}$ | |
| B. | 0.1 mol•L-1醋酸溶液中:c(H+)2=c (H+)•c(CH3COO-)+KW | |
| C. | 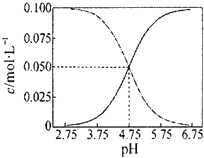 常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 等体积等物质的量浓度的CH3COONa(aq)与NaCl(aq)中离子总数大小:N前>N后 |
8.下列关于苯的说法中,正确的是( )
| A. | 苯不能使酸性KMnO4溶液褪色,属于饱和烃 | |
| B. | 常温下苯是一种易溶于水且密度比水小的液体 | |
| C. | 苯不具有典型的双键,故苯不能发生加成反应 | |
| D. | 苯分子为平面正六边形结构,6个碳原子之间的价键完全相同 |
5.某元素B的核电荷数为Z,已知Bn-和Am+的核外具有相同的电子层结构,则A元素的原子序数用Z、n、m来表示,应为( )
| A. | Z+n-m | B. | Z+m+n | C. | Z-n-m | D. | Z-n+m |
9.X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子数是最内层电子数的2倍;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子形成的-2价简单阴离子的核外电子排布与K+相同.下列有关这些元素性质的说法一定正确的是( )
| A. | X元素的氢化物的水溶液显碱性 | |
| B. | Y元素最高价氧化物的晶体具有很高的熔点和沸点 | |
| C. | Z元素的单质在一定条件下能与X元素的单质反应 | |
| D. | W元素的氧化物对应水化物均为强酸 |
7.28%的KOH溶液中,平均溶有一个OH-所需的水分子的个数为( )
| A. | 6个 | B. | 8个 | C. | 10个 | D. | 28个 |
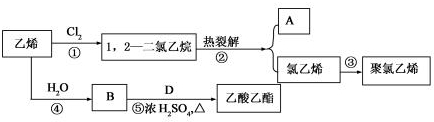
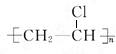 ,该反应类型是加聚反应
,该反应类型是加聚反应
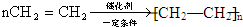 .
. 取1.38g由C、H、O三种元素组成的有机物A,在足量氧气中完全燃烧,若将燃烧产物通过碱石灰,碱石灰质量增加4.42g;若将燃烧产物通过浓硫酸,浓硫酸质量增加0.9g;已知:A的蒸气对氢气的相对密度为69.
取1.38g由C、H、O三种元素组成的有机物A,在足量氧气中完全燃烧,若将燃烧产物通过碱石灰,碱石灰质量增加4.42g;若将燃烧产物通过浓硫酸,浓硫酸质量增加0.9g;已知:A的蒸气对氢气的相对密度为69.