题目内容
7.下列说法不正确的是( )| A. | 在25℃时,将c mol•L-1的醋酸溶液与0.02mol•L-1NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=$\frac{2×{10}^{-9}}{c-0.02}$ | |
| B. | 0.1 mol•L-1醋酸溶液中:c(H+)2=c (H+)•c(CH3COO-)+KW | |
| C. | 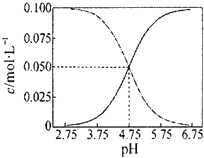 常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 等体积等物质的量浓度的CH3COONa(aq)与NaCl(aq)中离子总数大小:N前>N后 |
分析 A.溶液呈中性,则c(H+)=c(OH-)=10-7mol/L,c(Na+)=c(CH3COO-)=0.01mol/L,结合电离常数的表达式计算;
B.根据电荷守恒判断,醋酸溶液中存在c(H+)=c(OH-)+c(CH3COO-),结合c(H+)c(OH-)=Kw计算;
C.pH=4.75时c(CH3COOH)=c(CH3COO-),则pH=4.5溶液中:c(CH3COOH)>c(CH3COO-);
D.根据强碱弱酸盐发生水解以及电荷守恒来解答.
解答 解:A.呈中性则c(H+)=c(OH-)=10-7mol/L,c(Na+)=c(CH3COO-)=0.01mol/L,所以用含c的代数式表示CH3COOH的电离常数Ka=$\frac{1{0}^{-7}×0.01}{\frac{c}{2}-0.01}$=$\frac{2×1{0}^{-9}}{(c-0.02)}$mol•L-1,故A正确;
B.醋酸溶液中存在c(H+)=c(OH-)+c(CH3COO-),两边同乘以c(H+)可得c(H+)2=c (H+)•c(CH3COO-)+(H+)c(OH-)=c (H+)•c(CH3COO-)+KW,故B正确;
C.pH=4.75时c(CH3COOH)=c(CH3COO-),则pH=4.5溶液中:c(CH3COOH)>c(CH3COO-),溶液呈酸性,应存在c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-),故C正确;
D.醋酸是弱酸,所以CH3COONa溶液中发生水解反应:CH3COO--+H2O?CH3COOH+OH-,使溶液呈碱性,氢离子浓度小于10-7mol/L,所以NaCl溶液中c(Na+)+c(H+)大于CH3COONa溶液中c(Na+)+c(H+),根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(Cl-)可得溶液中离子总数为2×[c(Na+)+c(H+)]×V;同理可得CH3COONa溶液中总数为2×[c(Na+)+c(H+)]×V,所以NaCl溶液中离子总数大于CH3COONa溶液,即:N前<N后,故D错误.
故选D.
点评 本题考查了离子浓度大小比较、酸碱混合的定性判断等知识,题目难度中等,注意掌握盐的水解原理、酸碱混合的定性判断方法,能够根据电荷守恒、物料守恒、盐的水解原理判断溶液中各离子浓度大小.

| A. | CS2为V形的极性分子 | |
| B. | ClO3-的空间构型为平面三角形 | |
| C. | CO32-VSEPR模型名称与离子的立体构型名称不一致 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |
| A. | X2+2Y2?2XY2 | B. | 3X2+Y2?2X3Y | C. | X2+3Y2?2XY3 | D. | 2X2+2Y2?2X2Y |
①把A、B用导线连接后同时浸入稀硫酸中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸中,D发生还原反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.
上述四种金属的活动性顺序为( )
| A. | A>B>C>D | B. | C>A>B>D | C. | D>B>C>A | D. | B>A>C>D |
| A. | CH4、C2H2、C3H4 | B. | C2H6、C3H6、C4H6 | C. | C2H6、C3H6、C3H4 | D. | C2H4、C2H6、C3H6 |

 ,
, +CO2+H2O→
+CO2+H2O→ +NaHCO3,
+NaHCO3, +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
+3H2O.