题目内容
9.X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子数是最内层电子数的2倍;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子形成的-2价简单阴离子的核外电子排布与K+相同.下列有关这些元素性质的说法一定正确的是( )| A. | X元素的氢化物的水溶液显碱性 | |
| B. | Y元素最高价氧化物的晶体具有很高的熔点和沸点 | |
| C. | Z元素的单质在一定条件下能与X元素的单质反应 | |
| D. | W元素的氧化物对应水化物均为强酸 |
分析 X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质,X可能为O,也可能为N元素;Y元素原子最外电子数是最内层电子数的2倍,最外层电子数为4,所以Y为C或Si;Z元素+2价阳离子的核外电子排布与氖原子相同,则Z元素的质子数为10+2=12,故Z为Mg元素;W元素原子形成的-2价简单阴离子的核外电子排布与K+相同,W为S元素,据此解答.
解答 解:X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质,X可能为O,也可能为N元素;Y元素原子最外电子数是最内层电子数的2倍,最外层电子数为4,所以Y为C或Si;Z元素+2价阳离子的核外电子排布与氖原子相同,则Z元素的质子数为10+2=12,故Z为Mg元素;W元素原子形成的-2价简单阴离子的核外电子排布与K+相同,W为S元素.
A.X可能为O或N,氢化物可以是H2O、NH3、H2O2等,水是中性,H2O2溶液为酸性,故A错误;
B.Y为碳或Si,氧化物中二氧化硅属于原子晶体,具有很高的熔点和沸点,二氧化碳属于分子晶体,熔沸点较低,故B错误;
C.Mg在氧气中燃烧生成MgO,在氮气中燃烧生成Mg3N2,故C正确;
D.W为S元素,其氧化物对应水化物中硫酸为强酸,而亚硫酸属于弱酸,故D错误.
故选C.
点评 本题考查结构性质位置关系应用,注意元素的不确定性,利用列举法进行解答,熟练掌握元素化合物性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列有关化学用语或名称,表达错误的是( )
| A. | COCl2分子的结构式: | B. | 苯分子的比例模型: | ||
| C. | NaOH的电子式: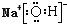 | D. |  的名称:2-乙基丁烷 的名称:2-乙基丁烷 |
17.常温常压下,将50mL三种气态烃的混合物与足量的氧气混合后点燃爆炸,恢复到原状态时,体积共减少了125mL,则三种烃可能是( )
| A. | CH4、C2H2、C3H4 | B. | C2H6、C3H6、C4H6 | C. | C2H6、C3H6、C3H4 | D. | C2H4、C2H6、C3H6 |
4.下列说法正确的是( )
| A. | 摩尔是一种国际基本物理量 | |
| B. | 标准状况下气体摩尔体积约为22.4 L | |
| C. | 氢的摩尔质量是2 g/mol | |
| D. | 在同温同压下,相同体积的任何气体单质所含分子数相同 |
14.下列实验装置图正确的是( )
| A. |  实验室制备及收集乙烯 | B. |  石油分馏 | ||
| C. | 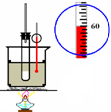 实验室制硝基苯 | D. | 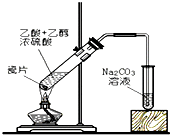 实验室制乙酸乙酯 |
18.下列物质:①乙醇②苯酚③乙醛④乙酸乙酯⑤丙烯酸(CH2═CH-COOH),其中与溴水、KMnO4酸性溶液、NaHCO3溶液都能反应的是( )
| A. | 仅⑤ | B. | 仅②④ | C. | 仅②⑤ | D. | 仅③⑤ |
2.下列化学式仅代表一种物质的是( )
| A. | CH4O | B. | C3H8O | C. | C3H6 | D. | C2H4O2 |