题目内容
12.乙烯是石油化学工业最重要的基础原料,经乙烯为原料可以制得许多工业材料和日用品.乙烯能发生下列转化关系: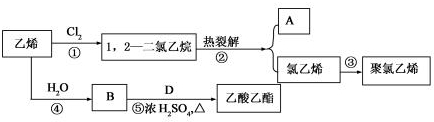
(1)A的分子为HCl,化合物D的官能团名称是羧基.
(2)写出反应③、⑤的化学方程式:
③n CH2=CHCl$\stackrel{引发剂}{→}$
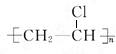 ,该反应类型是加聚反应
,该反应类型是加聚反应⑤CH3COOH+HOC2H5$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
(3)上述反应中,以生成有机产物为目标,原子利用率100%的反应有①和③④.
(4)甲同学在实验室制得的乙烯中含有少量的二氧化硫,于是设计实验进行验证,将生成的气体依次通过①品红溶液 ②NaOH溶液 ③品红溶液 ④溴的四氯化碳溶液.确定含有乙烯的现象为③中品红溶液不褪色,④中溴的四氯化碳溶液变为无色.
分析 乙烯与水发生加成反应生成B为CH3CH2OH,乙醇与D发生酯化反应生成乙酸乙酯,故D为CH3COOH.乙烯与氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生热裂解得到A与氯乙烯,则A为HCl,氯乙烯发生加聚反应生成聚氯乙烯,以此解答该题.
解答 解:乙烯与水发生加成反应生成B为CH3CH2OH,乙醇与D发生酯化反应生成乙酸乙酯,故D为CH3COOH.乙烯与氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生热裂解得到A与氯乙烯,则A为HCl,氯乙烯发生加聚反应生成聚氯乙烯,
(1)由上述分析可知,A的分子为HCl,化合物D为CH3COOH,官能团名称是:羧基,故答案为:HCl;羧基;
(2)氯乙烯发生加聚反应生成聚氯乙烯,反应化学方程式为:n CH2=CHCl$\stackrel{引发剂}{→}$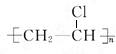 ,
,
反应⑤为乙醇、乙酸的酯化反应,方程式为CH3COOH+HOC2H5$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:n CH2=CHCl$\stackrel{引发剂}{→}$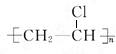 ;加聚反应;CH3COOH+HOC2H5$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;
;加聚反应;CH3COOH+HOC2H5$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;
(3)加成反应中原子利用率为100%,上述反应中①③④属于加成反应,以生成有机产物为目标,原子利用率100%的反应有①和③④,故答案为:③④.
(4)二氧化硫具有还原性,可与溴水、高锰酸钾反应,在检验乙烯之前应除去二氧化硫,二氧化硫具有酸性,可与碱反应,可用品红检验,如品红不褪色,且溴的四氯化碳溶液褪色,可说明含有乙烯,
故答案为:③中品红溶液不褪色,④中溴的四氯化碳溶液变为无色.
点评 本题考查有机物推断、为高考常见题型,侧重于学生的分析能力的考查,题目涉及石油化工、烯烃、醇、羧酸的性质与转化,题目基础性强,注意对基础知识的理解掌握.

| A. | X2+2Y2?2XY2 | B. | 3X2+Y2?2X3Y | C. | X2+3Y2?2XY3 | D. | 2X2+2Y2?2X2Y |
| A. | 电解时在阳极得到金属钠 | |
| B. | 在阴极附近的溶液中滴入酚酞溶液,溶液呈红色 | |
| C. | 在阴极附近有黄绿色的气体产生,并能使湿润淀粉碘化钾试纸变蓝 | |
| D. | 电解一段时间后,将电解液全部转移到烧杯中,充分搅拌后溶液呈中性 |
| A. | COCl2分子的结构式: | B. | 苯分子的比例模型: | ||
| C. | NaOH的电子式: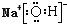 | D. |  的名称:2-乙基丁烷 的名称:2-乙基丁烷 |
| A. | CH4、C2H2、C3H4 | B. | C2H6、C3H6、C4H6 | C. | C2H6、C3H6、C3H4 | D. | C2H4、C2H6、C3H6 |
| A. | 摩尔是一种国际基本物理量 | |
| B. | 标准状况下气体摩尔体积约为22.4 L | |
| C. | 氢的摩尔质量是2 g/mol | |
| D. | 在同温同压下,相同体积的任何气体单质所含分子数相同 |
| A. | 标准状况下,11.2LCCl4所含的分子数为0.5NA | |
| B. | 7.8g苯分子中碳碳双键的数目为0.3NA | |
| C. | 常温常压下,4.2gC2H4和C9H18混合物中含有的碳原子数为0.3NA | |
| D. | 常温下,1molC3H8含有C-H共价键数为10NA |