题目内容
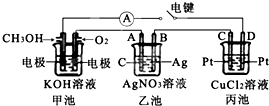 某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:(1)甲池中通入CH3OH电极的电极反应为
(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)甲池为原电池,燃料在负极失电子发生氧化还原反应在碱溶液中生成碳酸盐,结合电荷守恒写出电极反应;
(2)乙池是电解池,A为阳极,B为阴极,电池中是电解硝酸银溶液生成银,硝酸和氧气;
(3)乙池是电解池结合电子守恒计算消耗氧气的体积,丙为电解池C为阳极,D为阴极,电解氯化铜溶液铜离子在阴极得到电子析出铜.
(2)乙池是电解池,A为阳极,B为阴极,电池中是电解硝酸银溶液生成银,硝酸和氧气;
(3)乙池是电解池结合电子守恒计算消耗氧气的体积,丙为电解池C为阳极,D为阴极,电解氯化铜溶液铜离子在阴极得到电子析出铜.
解答:
解:(1)甲池为原电池,燃料在负极失电子发生氧化还原反应在碱溶液中生成碳酸盐,甲池中通入CH3OH电极的电极反应为:CH3OH-6e-+8OH-═CO32-+6H2O,
故答案为:CH3OH-6e-+8OH-═CO32-+6H2O;
(2)乙池是电解池,A为阳极,B为阴极,电池中是电解硝酸银溶液生成银,硝酸和氧气,电池反应为:4AgNO3+2H2O
4Ag+O2↑+4HNO3,
故答案为:阳极;4AgNO3+2H2O
4Ag+O2↑+4HNO3 ;
(3)当乙池中B极质量增加5.4g为Ag,物质的量=
=0.05mol,依据电子守恒计算4Ag~O2~4e-,甲池中理论上消耗O2的体积=
mol×22,4L/mol=0.28L=280ml;丙为电解池C为阳极,D为阴极,电解氯化铜溶液铜离子在阴极得到电子析出铜,结合电子守恒计算2Ag~Cu~2e-,析出铜质量=
×64g/mol=1.6g;
故答案为:280;D;1.6.
故答案为:CH3OH-6e-+8OH-═CO32-+6H2O;
(2)乙池是电解池,A为阳极,B为阴极,电池中是电解硝酸银溶液生成银,硝酸和氧气,电池反应为:4AgNO3+2H2O
| ||
故答案为:阳极;4AgNO3+2H2O
| ||
(3)当乙池中B极质量增加5.4g为Ag,物质的量=
| 5.4g |
| 108g/mol |
| 0.05 |
| 4 |
| 0.05 |
| 2 |
故答案为:280;D;1.6.
点评:本题考查了原电池电解池的相互串联问题,注意首先区分原电池和电解池,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在25℃下,将a mol?L-1的醋酸(HAc)与0.01mol?L-1的氢氧化钠溶液等体积混合,反应平衡时溶液呈中性.则下列说法中,不正确的是( )
| A、此时醋酸和氢氧化钠溶液恰好中和 | ||
| B、溶液中存在未电离的醋酸分子 | ||
C、用含a的代数式表示醋酸(HAc)的电离常数为Ka=
| ||
| D、a肯定大于0.01 |
下列事实不能用勒夏特列原理解释的是( )
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入NaOH溶液后,溶液颜色变浅 |
| B、对2HI(g)?H2(g)+I2(g)平衡体系,增大压强可使颜色变深 |
| C、反应CO+NO2?CO2+NO△H<0,升高温度可使平衡向逆反应方向移动 |
| D、工业合成氨工艺中,采用较高的压强来提高原料的转化率 |
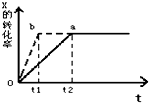 图中a曲线表示一定条件下的可逆反应:X(g)+Y(g)?2Z(g)+W(g);△H=QkJ/mol 的反应过程. 若使a曲线变为b曲线,可采取的措施是( )
图中a曲线表示一定条件下的可逆反应:X(g)+Y(g)?2Z(g)+W(g);△H=QkJ/mol 的反应过程. 若使a曲线变为b曲线,可采取的措施是( )| A、增大Y的浓度 |
| B、加入催化剂 |
| C、降低温度 |
| D、增大体系压强 |
一定量的盐酸和过量的铁粉反应,为了减缓反应速率,且不影响生成氢气的量,可向盐酸中加入适量的( )
| A、KNO3溶液 |
| B、K2CO3 溶液 |
| C、CuSO4 固体 |
| D、CH3COONa固体 |
下列对事实的说法、解释或结论正确的是( )
| A、酸根离子中不可能含有金属元素 |
| B、铁比铝容易生锈,是因为铁比铝活泼 |
| C、向某溶液中滴加KSCN溶液,溶液呈血红色,证明存在Fe3+而没有Fe2+ |
| D、铝箔在酒精灯火焰山加热熔化但不滴落,因为铝箔表面的氧化铝熔点高于铝 |
下列电离或水解方程式正确的是( )
| A、Na2SO3的水解:SO3 2-+2H2O?H2SO3+2OH- |
| B、NaHCO3的电离:NaHCO3?Na++H++CO3 2- |
| C、KHS的电离:KHS=K++HS- |
| D、NaClO溶液与FeCl2溶液混合:2ClO-+Fe2++2H2O=2HClO+Fe(OH)2↓ |
在地球上,氦元素主要以42He的形式存在,下列说法正确的是( )
| A、42He原子核内含有4个质子 |
| B、32He和42He互为同位素 |
| C、32He原子核内含有3个中子 |
| D、32He和42He是同一种核素 |