题目内容
一定量的盐酸和过量的铁粉反应,为了减缓反应速率,且不影响生成氢气的量,可向盐酸中加入适量的( )
| A、KNO3溶液 |
| B、K2CO3 溶液 |
| C、CuSO4 固体 |
| D、CH3COONa固体 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:减缓反应速率应使盐酸溶液的浓度降低,因铁粉过量,如不影响生成氢气的总量,则所加入物质不能改变酸溶液所能电离出的H+离子总物质的量,以此解答该题.
解答:
解:A.KNO3溶液在酸性条件下具有强氧化性,与铁反应不生成氢气,故A错误;
B.K2CO3 溶液与盐酸反应,影响生成氢气的总量,故B错误;
C.CuSO4固体与铁反应生成Cu,从而形成原电池加快反应速率,故C错误;
D.CH3COONa固体与盐酸反应生成弱电解质,溶液H+离子浓度降低,但不影响生成氢气的总量,故D正确.
故选D.
B.K2CO3 溶液与盐酸反应,影响生成氢气的总量,故B错误;
C.CuSO4固体与铁反应生成Cu,从而形成原电池加快反应速率,故C错误;
D.CH3COONa固体与盐酸反应生成弱电解质,溶液H+离子浓度降低,但不影响生成氢气的总量,故D正确.
故选D.
点评:本题考查化学反应速率的影响因素,为高考高频考点,侧重于基本概念的综合考查和运用,难度大不,注意把握题目要求以及影响反应速率的因素,学习中要注意相关基础知识的学习和积累.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
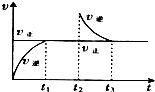 某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H>0,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )
某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H>0,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )| A、Z和W在该条件下一定不为气态 |
| B、t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C、若在该温度下此反应平衡常数表达式为K=C(X),则t1~t2时间段与t3时刻后的X浓度相等 |
| D、该反应的平衡常数K随温度升高而增大 |
取两份铝片,第一份与足量硫酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则两份铝片的质量之比为( )
| A、2:3 | B、1:1 |
| C、3:2 | D、1:3 |
可逆反应mA(g)?nB(g)+pC(s)△H=QKJ/moL,温度和压强的变化对正、逆反应速率的影响分别符合图中的两个图象,以下叙述正确的是( )


| A、m>n,Q>0 |
| B、m<n+p,Q>0 |
| C、m>n,Q<0 |
| D、m>n+p,Q<0 |
下列关于氯水的叙述,正确的是( )
| A、氯水中只含Cl2和H2O两种分子 |
| B、新制氯水只能使蓝色石蕊试纸变红 |
| C、光照氯水有气泡逸出,该气体是Cl2 |
| D、氯水放置数天后其pH将变小,酸性增强 |
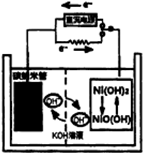 一种碳纳米管(氢气)二次电池原理如图.该电池的电解质为6moI/L KOH溶液,下列说法正确的是( )
一种碳纳米管(氢气)二次电池原理如图.该电池的电解质为6moI/L KOH溶液,下列说法正确的是( )| A、储存H2的碳纳米管放电时为负极,充电时为阳极 |
| B、充电时阳极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH- |
| C、放电时正极附近溶液的pH减小 |
| D、放电时负极反应为H2+2OH--2e-=2H2O |
下列说法不正确的是( )
①形成化学键的过程一定是化学变化
②离子化合物中一定含有金属元素
③物质有阳离子必有阴离子
④含有金属元素的离子一定为阳离子
⑤单质中一定含有共价键
⑥干冰升华破坏化学键
⑦HCI溶于水中电离出H+和Cl-,因此HCl中含有离子键.
①形成化学键的过程一定是化学变化
②离子化合物中一定含有金属元素
③物质有阳离子必有阴离子
④含有金属元素的离子一定为阳离子
⑤单质中一定含有共价键
⑥干冰升华破坏化学键
⑦HCI溶于水中电离出H+和Cl-,因此HCl中含有离子键.
| A、①②③④⑤⑥⑦ |
| B、②③④⑤⑥⑦ |
| C、③⑤⑥⑦ |
| D、①②③④⑤⑥ |
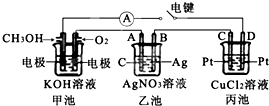 某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题: