题目内容
10.目前,关于二氧化碳是否为大气污染物有不同的观点:①二氧化碳是重要的化工原料 ②二氧化碳是植物光合作用的必需原料 ③二氧化碳是无色、无味、无毒的气体 ④除二氧化碳外,甲烷、一氧化二氮也是温室气体.认为“二氧化碳不是大气污染物”的理由是( )| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
分析 根据二氧化碳的工业应用、温室效应的气体成分分析.
解答 解:①二氧化碳是一种重要工业原料,可用在制纯碱、尿素、汽水等工业上,故①正确.
②二氧化碳的植物光合作用与环境污染无关,故②错误.
③二氧化碳虽是无色、无味、无毒的气体,但能产生温室效应,故③错误.
④除二氧化碳外,甲烷、一氧化二氮也是温室气体,故④正确.
故选B.
点评 本题考查环境污染及治理,为高频考点,侧重于化学与生活、生产、能源与环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
20.二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如图:
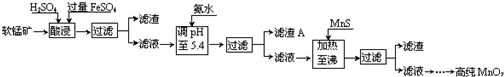
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
(1)FeSO4在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为2FeSO4+MnO2+2H2SO4=MnSO4+Fe2(SO4)3+2H2O.
(2)pH要调到5.4,应该使用pH计或精密pH试纸(填写仪器或试剂名称).滤渣A的主要成分是Fe(OH)3和Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.
(4)碱性锌锰电池中,MnO2参与的电极反应方程式为MnO2+H2O+e-=MnOOH+OH-.
(5)从废旧碱性锌锰电池中可以回收利用的物质有锌、二氧化锰(写两种).
(6)已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=2.79×103.

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(2)pH要调到5.4,应该使用pH计或精密pH试纸(填写仪器或试剂名称).滤渣A的主要成分是Fe(OH)3和Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.
(4)碱性锌锰电池中,MnO2参与的电极反应方程式为MnO2+H2O+e-=MnOOH+OH-.
(5)从废旧碱性锌锰电池中可以回收利用的物质有锌、二氧化锰(写两种).
(6)已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=2.79×103.
1.向下列液体中滴加稀硫酸,开始时生成沉淀,继续滴加稀H2SO4沉淀又溶解的是( )
| A. | Na2CO3溶液 | B. | BaCl2溶液 | C. | NaAlO2溶液 | D. | Fe(OH)3胶体 |
18.A、B、C、D、M均为中学化学常见物质,它们的转化关系如图所示(部分生成物和反应条件略去),其中A与H2O的反应在常温下进行,下列推断不正确的是( )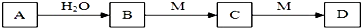
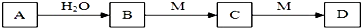
| A. | 若M为具有臭鸡蛋气味的气体,则D可能为酸式盐,且M(A)=M(C) | |
| B. | 若M为铁,则向D的溶液中通入A可能得C | |
| C. | 若C为纯碱,C转化为D的反应是CO32-+H2O+CO2═2HCO3-,则A可能为氯气 | |
| D. | 若M为可溶性铝盐,则A与水反应可能产生氢气,也可能产生氧气 |
15.下列溶液中各微粒的浓度关系不正确的是( )
| A. | 0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| B. | 等体积、等物质的量浓度的NaX和弱酸HX混合后呈酸性的溶液中:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) | |
| C. | 将0.2 mol•L-1 NaA溶液和0.1 mol•L-1盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)+c(OH-) | |
| D. | 1.5 L 0.1 mol•L-1 NaOH溶液中缓慢通入CO2至溶液增重4.4 g时,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
2.中草药秦皮中含有的七叶树内酯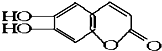 ,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )
,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )
 ,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )
,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )| A. | 3mol Br2;2mol NaOH | B. | 3mol Br2;4mol NaOH | ||
| C. | 2mol Br2;3mol NaOH | D. | 4mol Br2;4mol NaOH |
19.下列各组溶液,采用化学方法,不用其它试剂即可鉴别的是( )
| A. | CuSO4 NaCl | B. | NaHCO3 H2SO4 | ||
| C. | AlCl3 氨水 | D. | NaAlO2 HCl |
