题目内容
A元素原子M电子层上有3个电子,B元素与A元素的原子核外电子层数相同,B元素的原子最外层电子数为1.C元素在A元素的上一周期,C元素的最高价与最低价的代数和为0.
(1)A、B、C元素分别是 、 、 (填元素符号)
(2)B元素的最高价氧化物的水化物的电子式为 .
(3)C元素在周期表中的位置
(4)A和B的最高价氧化物的水化物相互反应的离子方程式为: .
(1)A、B、C元素分别是
(2)B元素的最高价氧化物的水化物的电子式为
(3)C元素在周期表中的位置
(4)A和B的最高价氧化物的水化物相互反应的离子方程式为:
考点:位置结构性质的相互关系应用
专题:
分析:A元素原子M电子层上有3个电子,则A为Al;B元素与A元素的原子核外电子层数相同,B元素的原子最外层电子数为1,则B为Na;C元素在A元素的上一周期,C元素的最高价与最低价的代数和为0,处于ⅣA族,则C为碳元素.
解答:
解:A元素原子M电子层上有3个电子,则A为Al;B元素与A元素的原子核外电子层数相同,B元素的原子最外层电子数为1,则B为Na;C元素在A元素的上一周期,C元素的最高价与最低价的代数和为0,处于ⅣA族,则C为碳元素,
(1)由上述分析可知,A、B、C的元素符号分别是:Al、Na、C,故答案为:Al;Na;C;
(2)B元素的最高价氧化物的水化物为NaOH,电子式为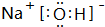 ,故答案为:
,故答案为: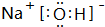 ;
;
(3)C为碳元素,元素在周期表中的位置:第二周期ⅣA族,故答案为:第二周期ⅣA族;
(4)A和B的最高价氧化物的水化物分别为Al(OH)3、NaOH,相互反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O.
(1)由上述分析可知,A、B、C的元素符号分别是:Al、Na、C,故答案为:Al;Na;C;
(2)B元素的最高价氧化物的水化物为NaOH,电子式为
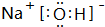 ,故答案为:
,故答案为: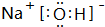 ;
;(3)C为碳元素,元素在周期表中的位置:第二周期ⅣA族,故答案为:第二周期ⅣA族;
(4)A和B的最高价氧化物的水化物分别为Al(OH)3、NaOH,相互反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,侧重对基础知识的巩固.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法不正确的是( )
| A、化合物BmAm分子中所有原子一定共平面 |
| B、一定条件下,元素C、D、E的最高价氧化物对应的水化物之间能发生反应 |
| C、工业上常用电解法制备元素C、D、E的单质 |
| D、化合物BAn与BEn具有相同类型的化学键 |
“玉兔号”巡月器的发动机套有一件“土豪金”外衣-耐高温,抗震复合材料,该复合材料以硅酸铝纤维(Al2O3-SiO2)为基体,六钛酸钾晶须(K2O?6TiO2)为增强剂.下列说法中正确的是( )
| A、该复合材料属于新型有机非金属材料 |
| B、Al、K、Ti都属于主族元素 |
| C、原子半径:K>Si>O |
| D、该复合材料能耐强酸和强碱腐蚀 |
 某温度下的溶液中c(H+)=1.0×10 x mol/L,c(OH-)=1.0×10 y mol/L.x与y的关系如图所示.请回答下列问题:
某温度下的溶液中c(H+)=1.0×10 x mol/L,c(OH-)=1.0×10 y mol/L.x与y的关系如图所示.请回答下列问题:


 :
:
 A~G是前四周期除稀有气体之外原子序数依次增大的七种元素.A与其它元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.请结合题目回答以下问题:
A~G是前四周期除稀有气体之外原子序数依次增大的七种元素.A与其它元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.请结合题目回答以下问题: