题目内容
9.下列说法正确的是( )| A. | 电解MgCl2饱和溶液,可制得金属镁 | |
| B. | 采用牺牲阳极的阴极保护法:在海轮外壳连接锌块保护外壳 | |
| C. | 金属在潮湿空气中腐蚀的实质是:M+nH2O═M(OH)n+$\frac{n}{2}$ H2↑ | |
| D. | 地下钢管与外加直流电源的正极相连以保护它不受腐蚀 |
分析 A.电解MgCl2饱和溶液生成氢氧化镁;
B.原电池中负极失电子被腐蚀,正极被保护;
C.金属在潮湿的空气中发生吸氧腐蚀而变质;
D.电解池的阳极上发生失电子的氧化反应.
解答 解:A.电解MgCl2饱和溶液生成氢氧化镁,电解熔融的氯化镁可以制得Mg,故A错误;
B.原电池中负极失电子被腐蚀,正极被保护,所以在海轮外壳连接锌块保护外壳,Zn失电子作负极,Fe作正极被保护,属于牺牲阳极的阴极保护法,故B正确;
C.金属在潮湿的空气中发生吸氧腐蚀而变质,吸氧腐蚀不生成氢气,故C错误;
D.地下钢管与外加直流电源的正极相连,Fe作阳极失电子,被腐蚀,所以不能保护它不受腐蚀,故D错误.
故选B.
点评 本题考查了电解原理的应用、金属腐蚀与防护,明确金属腐蚀原理是解本题关键,知道析氢腐蚀和吸氧腐蚀的区别及其原因,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列反应的离子方程式中,书写正确的是( )
| A. | 钠跟水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向硫酸溶液中加入Ba(OH)2溶液:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| C. | 向A12(SO4)3溶液中加入过量的氨水:A13++3NH3•H2O═A1(OH)3↓+3NH4+ | |
| D. | FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
20.铝制品抗腐蚀性极强,原因是( )
| A. | 铝的金属活动性极差 | B. | 空气中没有能与铝反应的物质 | ||
| C. | 其表面的氧化膜致密 | D. | 铝制品被人为地进行了防腐处理 |
17.下列关于化学反应限度的说法中不正确的是( )
| A. | 当一个可逆反应达到平衡状态时,这就是这个反应在该条件下所能达到的限度 | |
| B. | 可逆反应是指同一条件下,既能向正反应方向进行,又能向逆反应方向同时进行的反应 | |
| C. | 平衡状态的本质是各反应物、生成物的分子个数不再随时间改变而改变 | |
| D. | 金属钠在氧气中燃烧瞬间达到平衡状态 |
14.已知反应4CO+2NO2?N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最慢的是( )
| A. | v(CO)=1.5 mol•L-1•min-1 | B. | v(NO2)=0.7 mol•L-1•min-1 | ||
| C. | v(N2)=0.4 mol•L-1•min-1 | D. | v(CO2)=1.1 mol•L-1•min-1 |
1.某市高速公路发生苯酚槽罐车泄漏事故,导致部分苯酚泄漏并造成污染.下列对于苯酚的叙述中,错误的是( )
| A. | 苯酚是一种弱酸,滴加指示剂不变色 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 碳酸氢钠溶液中滴入苯酚的水溶液后会放出二氧化碳 | |
| D. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 |
19.X元素的化合价为+m价,Y元素的化合价为-n价,那么X和Y组成的化合物的一个分子中,原子个数( )
| A. | 一定是m个 | B. | 一定是n个 | C. | 一定是(m+n)个 | D. | 可能是(m+n)个 |

 (R、R′可表示烃基或官能团)
(R、R′可表示烃基或官能团) .
.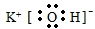 ;CO2
;CO2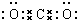 .
.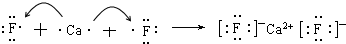 .
.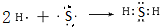 .
.