题目内容
3.潜艇中常用的供氧剂是( )| A. | Na2CO3 | B. | Na2O | C. | Na2O2 | D. | KClO3 |
分析 过氧化钠能与二氧化碳反应生成氧气角度考虑,装置简单,反应在常温下进,与CO2反应产生供人呼吸的氧气.
解答 解:Na2O2与二氧化碳反应生成碳酸钠和氧气,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2;与我们学过的制氧气方法相比,过氧化钠作为呼吸面具和潜水艇的供氧剂,装置简单,反应能在常温下进行;与CO2反应产生供人呼吸的氧气,碳酸钠、氧化钠、氯酸钾等物质不具有次性质,故选C.
点评 本题考查了过氧化钠性质分析,该实验题具有实际意义,属于身边的化学,要平时多留心,多积累,做到触类旁通,题目较简单.

练习册系列答案
相关题目
14.下列各电离方程式中,书写正确的是( )
| A. | H2S?2H++S2- | B. | KHSO4?K++H++SO42- | ||
| C. | Al(OH)3?Al3++3OH- | D. | HClO═H++ClO- |
11.下列表达方式错误的是( )
| A. | CO2的比例模型: | |
| B. | 甲烷的电子式 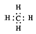 | |
| C. | 硫离子的核外电子排布式 1s22s22p63s23p4 | |
| D. | 碳-12原子构成${\;}_6^{12}$C |
18.下列事实不能用平衡移动原理解释的是( )
| A. | 工业合成氨时选择500℃ | |
| B. | 配制FeCl3溶液时加入少量的盐酸 | |
| C. | 在Na2CO3溶液中,由水电离出的c(OH-)>1×10-7mol/L | |
| D. | AgCl在水中的溶解度大于在饱和NaCl溶液中的溶解度 |
8.下列离子方程式,书写正确的是( )
| A. | 碳酸钙和盐酸反应 CO32-+2H+=H2O+CO2↑ | |
| B. | 向氢氧化钡溶液中加硫酸溶液 Ba2++SO42-=BaSO4↓ | |
| C. | 碳酸氢钙溶液与盐酸溶液反应 HCO3-+H+=H2O+CO2↑ | |
| D. | 向稀盐酸溶液中加铁粉 3Fe+6H+=2Fe3++3H2↑ |
12.下列实验可行的是( )
| A. | 用饱和Na2CO3溶液除去CO2中混有的HCl气体 | |
| B. | 用量筒量取20.83mL12mol/L的浓硫酸配制250mL1mol/L稀硫酸 | |
| C. | 用浓硫酸干燥CO2、SO2、HI等酸性气体 | |
| D. | 用稀HNO3能鉴别Mg、Na2CO3、NaAlO2、Na2SiO3四种固体 |
13.已知:Na2SO3+H2SO4═Na2SO4+SO2↑+S↓+H2O某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(1)该实验①、②可探究温度对反应速率的影响,因此 V3是0;
(2)实验①、③可探究浓度对反应速率的影响,因此V5是6.0.
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(2)实验①、③可探究浓度对反应速率的影响,因此V5是6.0.