题目内容
11.下列表达方式错误的是( )| A. | CO2的比例模型: | |
| B. | 甲烷的电子式 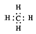 | |
| C. | 硫离子的核外电子排布式 1s22s22p63s23p4 | |
| D. | 碳-12原子构成${\;}_6^{12}$C |
分析 A.二氧化碳分子中含有两个碳氧双键,为直线型结构;
B.甲烷为共价化合物,分子中含有4个碳氢键,碳原子最外层满足8电子稳定结构;
C.硫离子核外电子总数为18,最外层满足8电子稳定结构;
D.碳-12的质量数为12、质子数为6.
解答 解:A.二氧化碳的分子式为CO2,由模型可知小球为碳原子,2个大球为氧原子,氧原子半径大,实际碳原子半径大于氧原子半径,其正确的比例模型为: ,故A错误;
,故A错误;
B.甲烷为共价化合物,分子中含有4个C-H键,其电子式为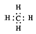 ,故B正确;
,故B正确;
C.硫离子的3p电子层含有6个电子,其正确的核外电子排布式为:1s22s22p63s23p6,故C错误;
D.碳-12原子的质子数为6、质量数为12,该原子的表示方法为:${\;}_6^{12}$C,故D正确;
故选AC.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及比例模型、电子式、电子排布式、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
16.在强酸性溶液中能大量共存的无色透明离子组是( )
| A. | Mg2+ Na+ Cl- SO42- | B. | K+ Na+ CO32- NO3- | ||
| C. | K+ Na+ Cl- Cu2+ | D. | Na+Ba2+OH- SO42- |
3.潜艇中常用的供氧剂是( )
| A. | Na2CO3 | B. | Na2O | C. | Na2O2 | D. | KClO3 |
20.如表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①N,⑥Si.
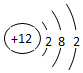
(2)画出原子的结构示意图:④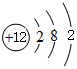 ,⑤
,⑤ .
.
(3)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.(均用元素符号表示)
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.(均写出物质的化学式)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:④
 ,⑤
,⑤ .
.(3)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.(均用元素符号表示)
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.(均写出物质的化学式)
 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
 M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题: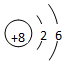 、
、