题目内容
16.a L H2和CO的混合气体,充分燃烧后,消耗同温同压下氧气的体积是( )| A. | a L | B. | $\frac{a}{2}$ L | C. | $\frac{a}{3}$ L | D. | 无法计算 |
分析 发生反应:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,由方程式可知消耗氧气体积为CO和H2的混合总体积的$\frac{1}{2}$,以此解答该题.
解答 解:发生反应:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,由方程式可知消耗氧气体积为CO和H2的混合总体积的$\frac{1}{2}$,
即消耗氧气体积为a L×$\frac{1}{2}$=$\frac{a}{2}$ L,
故选B.
点评 本题考查混合物反应有关计算,明确发生反应即可解答,旨在考查学生分析计算能力,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列关于乙烯的叙述中不正确的是( )
| A. | 无色气体,难溶于水,密度比空气略小 | |
| B. | 乙烯燃烧时,火焰明亮,同时产生黑烟 | |
| C. | 与溴水发生取代反应而使溴水褪色 | |
| D. | 乙烯的产量标志着一个国家的石油化工水平 |
1.下列有关阿伏加德罗常数(NA)的说法错误的是( )
| A. | 32g O2所含的原子数目为NA | |
| B. | 0.5mol H2O含有的原子数目为1.5NA | |
| C. | 1mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氧气分子的物质的量是0.5mol |
18.大气中硫、氮的氧化物是形成酸雨的主要物质.某地酸雨中可能含有下列离子:Na+、Ba2+、NH4+、Al3+、Cl-、SO32-、SO42-、NO3-等.某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成3份,进行如下实验:
请回答下列问题:(1)判断该酸雨中肯定不存在的离子是SO32-、Ba2+
(2)写出试液中滴加淀粉KI溶液时发生反应的离子方程式:6I-+2NO3-+8H+=2NO↑+3I2+4H2O
(3)第三份试液滴加NaOH溶液,加热整个过程中有多个反应,写出其中一个反应的离子方程式OH-+H+=H2O,NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O.
(4)设计实验方案,检验该溶液中是否存在Cl-:少量试液滴加足量的Ba(NO3)2溶液,静置取上层澄清液加HNO3酸化的AgNO3溶液,若有白色沉淀生成,则证明存在Cl-.
(5)该小组为了探究NO参与硫酸型酸雨的形成过程,在烧瓶中充入含有少量NO的SO2气体,再慢慢通入O2,发生化学反应后,再喷洒适量蒸馏水即得硫酸型酸雨,则NO在上述反应中的作用是催化剂.
| 试样 | 所加试剂 | 实验现象 |
| 第一份试液 | 滴加适量的淀粉KI溶液 | 呈蓝色 |
| 第二份试液 | 滴加用盐酸酸化的BaCl2溶液 | 有白色沉淀 |
| 第三份试液 | 滴加NaOH溶液,加热,加入的NaOH溶液体积(V)与生成的沉淀、产生的气体(n)的关系如右图 |  |
(2)写出试液中滴加淀粉KI溶液时发生反应的离子方程式:6I-+2NO3-+8H+=2NO↑+3I2+4H2O
(3)第三份试液滴加NaOH溶液,加热整个过程中有多个反应,写出其中一个反应的离子方程式OH-+H+=H2O,NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O.
(4)设计实验方案,检验该溶液中是否存在Cl-:少量试液滴加足量的Ba(NO3)2溶液,静置取上层澄清液加HNO3酸化的AgNO3溶液,若有白色沉淀生成,则证明存在Cl-.
(5)该小组为了探究NO参与硫酸型酸雨的形成过程,在烧瓶中充入含有少量NO的SO2气体,再慢慢通入O2,发生化学反应后,再喷洒适量蒸馏水即得硫酸型酸雨,则NO在上述反应中的作用是催化剂.

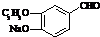 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$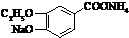 +2Ag↓+3NH3+H2O或
+2Ag↓+3NH3+H2O或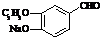 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$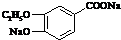 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.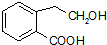 .
. 合成
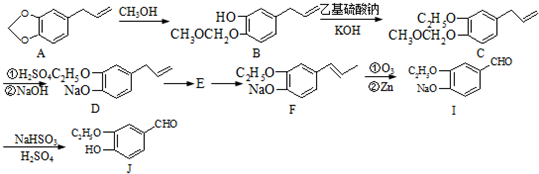
合成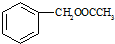 合成路线流程图示例如下:
合成路线流程图示例如下: