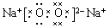题目内容
1.下列有关阿伏加德罗常数(NA)的说法错误的是( )| A. | 32g O2所含的原子数目为NA | |
| B. | 0.5mol H2O含有的原子数目为1.5NA | |
| C. | 1mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氧气分子的物质的量是0.5mol |
分析 A.每个氧分子中含2个原子,根据N(O)=2 $\frac{m({O}_{2})}{M({O}_{2})}$NA计算判断;
B.1mol水分子中含2molH原子和1molO原子;
C.1mol H2O含有的H2O分子1mol,n=$\frac{N}{{N}_{A}}$;
D.n=$\frac{N}{{N}_{A}}$计算氧气分子物质的量.
解答 解:A.每个氧分子中含2个原子,N(O)=2$\frac{m({O}_{2})}{M({O}_{2})}$NA=2$\frac{32g}{32g/mol}$NA=2NA,32g O2所含的原子数目为2NA ,故A错误;
B.0.5mol H2O含有的原子数目=0.5mol×3×NA=1.5NA ,故B正确;
C.1mol H2O含有的H2O分子数目=1mol×NA=NA ,故C正确;
D.0.5NA个氧气分子的物质的量=$\frac{0.5{N}_{A}}{{N}_{A}}$=0.5mol,故D正确;
故选A.
点评 本题考查了阿伏伽德罗常数的简单计算,题目难度不大,注意熟练掌握阿伏伽德罗常数与物质的量、摩尔质量之间的转化关系,试题能够培养学生灵活应用所学知识的能力.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
11.已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法.
【方法一】还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.具体流程如下:

有关离子完全沉淀的pH如下表:
(1)写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式Cr2O72-+6Fe2++14H+═2 Cr3++6Fe3++7H2O.
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.则在操作②中可用于调节溶液pH的试剂为:C(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
【方法二】电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-.
(5)电解法中加入氯化钠的作用是:增强溶液导电性.
【方法一】还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.具体流程如下:

有关离子完全沉淀的pH如下表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.则在操作②中可用于调节溶液pH的试剂为:C(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
【方法二】电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-.
(5)电解法中加入氯化钠的作用是:增强溶液导电性.
9.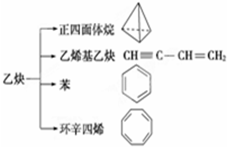 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )| A. | 正四面体烷的分子式为C4H4,其二氯代物有两种 | |
| B. | 苯为平面六边形结构,分子中存在C-C和C═C,能使酸性KMnO4溶液褪色 | |
| C. | 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同 | |
| D. | 环辛四烯跟苯的结构很像,不能使溴水褪色 |
16.a L H2和CO的混合气体,充分燃烧后,消耗同温同压下氧气的体积是( )
| A. | a L | B. | $\frac{a}{2}$ L | C. | $\frac{a}{3}$ L | D. | 无法计算 |
6.可以鉴别葡萄糖溶液的试剂是( )
| A. | 银氨溶液 | B. | 氢氧化铜固体 | C. | 石蕊试液 | D. | 碳酸钠溶液 |
3.有5种元素X、Y、Z、Q、T.X原子M层上有2个未成对电子且M层无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的P能级上只有一对成对电子;T原子的M电子层上p轨道半充满.下列叙述不正确的是( )
| A. | 元素Y和Q可形成化合物Y3Q4 | |
| B. | T和Z各有一种单质的空间构型为正四面体形,键角都是109°28? | |
| C. | X和Q结合生成的化合物可以形成离子化合物 | |
| D. | ZQ2是极性键构成的非极性分子 |
4.下列有关化学键的说法正确的是( )
| A. | 离子化合物中一定含有离子键,共价化合物中可能含有离子键 | |
| B. | 共价化合物中一定含有共价键,离子化合物中可能含有共价键 | |
| C. | 由非金属元素形成的化合物中一定只含共价键 | |
| D. | 含有金属元素的化合物中一定含有离子键 |