题目内容
4.由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体.请回答:
(1)写出固体A与液体X反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑.
(2)气体Y是一种大气污染物,直接排放会形成酸雨.可用溶液B吸收,写出过量的Y与B溶液反应的离子方程式SO2+OH-=HSO3-
(3)若气体C与Y在恒容绝热的条件下反应,下列哪些说法说明该反应达到平衡状态:ABD
A.温度不变 B.2v正(C)=v逆(Y)
C.混合气体的密度不变 D.混合气体的平均相对分子质量不变.
分析 A是一种淡黄色固体,则A为Na2O2,能与液态X反应生成气体C与B的溶液,可推知X为H2O、B为NaOH、C为O2,
(1)过氧化钠和水反应生成NaOH和氧气;
(2)气体Y是一种大气污染物,直接排放会形成酸雨,则Y是二氧化硫,过量的Y与B溶液完全反应时,所得溶液D为NaHSO3;
(3)当反应前后改变的物理量不变时,该反应达到平衡状态,据此判断.
解答 解:A是一种淡黄色固体,则A为Na2O2,能与液态X反应生成气体C与B的溶液,可推知X为H2O、B为NaOH、C为O2,
(1)过氧化钠和水反应生成NaOH和氧气,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,
故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑;
(2)体Y是一种大气污染物,直接排放会形成酸雨.可用溶液B吸收,是二氧化硫被氢氧化钠溶液吸收,过量二氧化硫和氢氧化钠溶液反应生成亚硫酸氢钠,反应的离子方程式为:SO2+OH-=HSO3-,
故答案为:SO2+OH-=HSO3-;
(3)当反应前后改变的物理量不变时,该反应达到平衡状态,该可逆反应前后改变的物理量有温度、压强、平均分子量,所以当温度、压强、混合气体的平均分子量不变时,该反应达到平衡状态,若气体C与Y在恒容绝热的条件下反应,2SO2+O2?2SO3,
A.反应过程中一定伴随能量变化,恒容绝热的条件下当温度不变说明反应达到平衡状态,故A正确;
B.反应速率之比等于化学方程式计量数之比为正反应速率之比,当2v正(C)=v逆(Y),说明Y的正逆反应速率相同,反应达到平衡状态,故B正确;
C.反应前后气体质量和体积不变,混合气体的密度始终不变,密度不变不能说明反应达到平衡状态,故C错误;
D.反应前后气体质量不变,物质的量减小,当混合气体的平均相对分子质量不变说明反应达到平衡状态,故D正确;
故答案为:ABD.
点评 本题考查了无机物推断及元素周期表、元素周期律的综合应用,综合性较强,涉及元素化合物知识、化学反应原理、化学用语等知识点,难点是化学平衡状态判断,注意题干中限制性信息,为易错点.

 阅读快车系列答案
阅读快车系列答案| A. | 氡是双原子分子 | |
| B. | 氡气因其化学性质活泼而对人体有害 | |
| C. | 氡气因其具有放射性而对人体有害 | |
| D. | 222Rn、219Rn、220Rn互为同素异形体 |
①苯不能使酸性KMnO4溶液褪色
②苯不能使溴水因化学反应而褪色
③经实验测定只有一种结构的邻二甲苯
④苯能在加热和催化剂条件下氢化成环己烷
⑤苯中相邻C原子与C原子间的距离都相等.
| A. | 只有①②③⑤ | B. | 只有④⑤ | C. | ①②③④⑤ | D. | 只有①② |
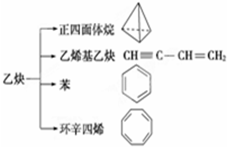 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )| A. | 正四面体烷的分子式为C4H4,其二氯代物有两种 | |
| B. | 苯为平面六边形结构,分子中存在C-C和C═C,能使酸性KMnO4溶液褪色 | |
| C. | 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同 | |
| D. | 环辛四烯跟苯的结构很像,不能使溴水褪色 |
| A. | a L | B. | $\frac{a}{2}$ L | C. | $\frac{a}{3}$ L | D. | 无法计算 |
| A. | 银氨溶液 | B. | 氢氧化铜固体 | C. | 石蕊试液 | D. | 碳酸钠溶液 |
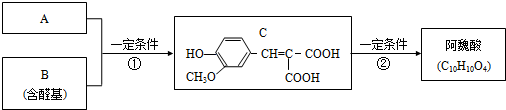
 ;
; ;
;