题目内容
19.设NA表示阿伏加德罗常数的数值,下列叙述正确的是( )| A. | 同温同压下,相同体积的氟气和氩气所含的原子数相等 | |
| B. | 标准状况下,1.12 L NO与1.12 L O2的混合物中含有的原子数为0.2NA | |
| C. | 常温下,1L 0.1 mol•L-1 CuSO4溶液中含有的Cu2+数目为0.1NA | |
| D. | 25℃时,1L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
分析 A、氟气为双原子分子,而氩气为单原子分子;
B、求出两种气体的物质的量,然后根据NO和氧气均为双原子分子来分析;
C、铜离子为弱碱阳离子,在溶液中会水解;
D、pH=13的氢氧化钡溶液中,氢氧根的浓度为0.1mol/L.
解答 解:A、同温同压下,相同体积的氟气和氩气的物质的量相同,但氟气为双原子分子,而氩气为单原子分子,故两者中含有的原子数不同,故A错误;
B、标况下1.12LNO和1.12L氧气的物质的量均为0.05mol,而NO和氧气均为双原子分子,故0.05molNO和0.05mol氧气中含有的原子均为0.1NA个,两者混合后根据原子个数守恒可知,原子个数共为0.2NA个,故B正确;
C、铜离子为弱碱阳离子,在溶液中会水解,故溶液中的铜离子的个数小于0.1NA个,故C错误;
D、pH=13的氢氧化钡溶液中,氢氧根的浓度为0.1mol/L,故1L溶液中含有的氢氧根的个数为0.1NA个,故D正确.
故选BD.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
10.下列各组给定原子序数的元素,不能形成原子个数之比为1:1共价化合物的是( )
| A. | 3和17 | B. | 1和8 | C. | 6和8 | D. | 1和9 |
7.3.2g铜与过量的硝酸(8mol•L-1,60mL)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+离子为nmol.此时溶液中所含NO3-的物质的量为( )
| A. | 0.28mol | B. | 0.3lmol | C. | (n+0.2)mol | D. | (n+0.1)mol |
14.重水(D2O)的主要作用是作为核反应堆的减速剂,下列说法正确的是( )
| A. | 氘(D)原子核外有2个电子 | B. | 1H与D互称同位素 | ||
| C. | H2与D2互称同素异形体 | D. | 18g D2O的物质的量为1mol |
8.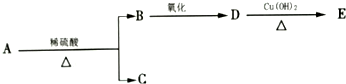 分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有( )
分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有( )
 分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有( )
分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有( )| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
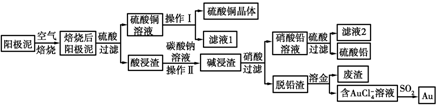
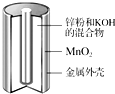 碱性锌锰干电池是生活中应用最普遍的电池之一,其结构如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH.
碱性锌锰干电池是生活中应用最普遍的电池之一,其结构如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH.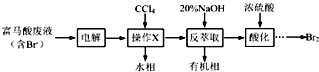

 .
.