题目内容
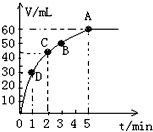 加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.(忽略溶液体积变化)
加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.(忽略溶液体积变化)(1)计算初始时溶液中过氧化氢的物质的量浓度
(2)A、B、C、D各点反应速率快慢的顺序为
(3)列式计算反应开始时到2min放出45mLO2时,H2O2的质量分数
考点:化学反应速率变化曲线及其应用
专题:
分析:(1)根据图片知,双氧水发生反应2H2O2
2H2O+O2↑,n(O2)=
=0.0027mol,根据双氧水和氧气的关系式得n(H2O2)=2n(O2)=2×0.0027mol=0.0054mol,根据C=
计算过氧化氢的物质的量浓度;
(2)v=
知,相同时间内,反应速率与体积变化量成正比;反应物浓度越大,反应速率越大;
(3)反应开始时到2min放出45mLO2时,n(O2)=
=0.002mol,m(O2)=0.002mol×32g/mol=0.064g,原来溶液质量=1.1g/mL×50mL=55g,2min时溶液质量=55g-0.064g=54.36g,根据质量分数公式计算其质量分数.
| ||
| 0.06L |
| 22.4L/mol |
| n |
| V |
(2)v=
| △V |
| △t |
(3)反应开始时到2min放出45mLO2时,n(O2)=
| 0.045L |
| 22.4L/mol |
解答:
解:(1)根据图片知,双氧水发生反应2H2O2
2H2O+O2↑,n(O2)=
=0.0027mol,根据双氧水和氧气的关系式得n(H2O2)=2n(O2)=2×0.0027mol=0.0054mol,物质的量浓度=
=
=0.11mol/L,
故答案为:0.11mol/L;
(2)v=
知,相同时间内,反应速率与体积变化量成正比,根据图片知,反应速率大小顺序是D>C>B>A;反应物浓度越大,反应速率越大,随着反应的进行,反应物浓度逐渐减小,则反应速率逐渐减小,故答案为:D>C>B>A;随着反应的进行,c(H2O2)逐渐降低,反应速率逐渐变慢;
(3)反应开始时到2min放出45mLO2时,n(O2)=
=0.002mol,m(O2)=0.002mol×32g/mol=0.064g,原来溶液质量=1.1g/mL×50mL=55g,2min时溶液质量=55g-0.064g=54.36g,双氧水的质量=(0.0054mol-0.004mol)×34g/mol=0.0048g,
其质量分数=
×100%=0.086%,故答案为:0.086%.
| ||
| 0.06L |
| 22.4L/mol |
| n |
| V |
| 0.0054mol |
| 0.05L |
故答案为:0.11mol/L;
(2)v=
| △V |
| △t |
(3)反应开始时到2min放出45mLO2时,n(O2)=
| 0.045L |
| 22.4L/mol |
其质量分数=
| 0.048g |
| 54.36g |
点评:本题以根据方程式的有关计算为载体考查反应速率的问题,侧重考查分析、计算能力,知道反应速率的影响因素、质量分数公式、物质的量浓度公式等即可解答,题目难度不大.

练习册系列答案
相关题目
下列属于电解质并能导电的物是( )
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤NaCl晶体 ⑥盐酸.
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤NaCl晶体 ⑥盐酸.
| A、① | B、①②③⑤⑥ |
| C、①②⑥ | D、①③④⑤ |
2013年1月28日日本岛发生火山喷发,将滚热的云状火山气体和火山灰喷向高空.火山气体主要包括①水蒸气②CO2③SO2④SO3⑤HCl,这些气体对环境造成了极大的危害,对①~⑤中的相关气体的叙述中不正确的是( )
| A、收集一定量的火山气体通入足量BaCl2溶液中,只能生成BaSO4一种沉淀 |
| B、②③④属于酸性氧化物 |
| C、⑤属于强电解质 |
| D、①②③④属于非电解质 |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
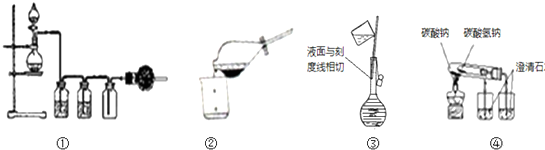

| A、①可用于实验室用MnO2固体与浓盐酸反应,制取并收集干燥、纯净的Cl2 |
| B、②从溴水中萃取溴后的分离操作 |
| C、③配制1mol/LNaCl溶液定容操作 |
| D、用图④操作可比较Na2CO3与NaHCO3的热稳定性 |