题目内容
由Fe、CuO、C、Al组成的混合粉末,取样品进行下列实验(部分产物略去):

(1)反应1中的化学方程式是: ;
(2)反应2中的离子方程式是: .
(3)当溶液B变成溶液C时双氧水变成了水,请完成该反应的离子方程式(配平的化学计量数写在方框内,若计量数为“1”也要写出来).
□Fe2++□H2O2+□H+=□Fe3++□H2O,此该反应的还原剂为 .
(4)已知固体B与浓硫酸共热可以产生两种气体,若反应后硫酸变成SO2,则1.5mol硫酸完全反应转移的电子数为 mol.

(1)反应1中的化学方程式是:
(2)反应2中的离子方程式是:
(3)当溶液B变成溶液C时双氧水变成了水,请完成该反应的离子方程式(配平的化学计量数写在方框内,若计量数为“1”也要写出来).
□Fe2++□H2O2+□H+=□Fe3++□H2O,此该反应的还原剂为
(4)已知固体B与浓硫酸共热可以产生两种气体,若反应后硫酸变成SO2,则1.5mol硫酸完全反应转移的电子数为
考点:物质分离和提纯的方法和基本操作综合应用
专题:化学实验基本操作
分析:由Fe、CuO、C、Al组成的混合粉末加入过量氢氧化钠溶液过滤得到固体A为C、Fe、CuO,溶液A为NaAlO2,固体A加入过量稀硫酸过滤得到固体B为C,滤液B为FeSO4,CuSO4,加入过氧化氢氧化亚铁离子为铁离子;
(1)反应1是铝和氢氧化钠溶液反应生成偏铝酸钠和氢气;
(2)反应2为铁和稀硫酸反应生成硫酸亚铁和氢气,氧化铜和稀硫酸反应生成硫酸铜和水;
(3)当溶液B变成溶液C时双氧水变成了水,是过氧化氢氧化亚铁离子为铁离子;
(4)固体B为C,C和浓硫酸加热反应生成二氧化碳、二氧化硫和水,结合化学方程式定量关系计算电子转移;
(1)反应1是铝和氢氧化钠溶液反应生成偏铝酸钠和氢气;
(2)反应2为铁和稀硫酸反应生成硫酸亚铁和氢气,氧化铜和稀硫酸反应生成硫酸铜和水;
(3)当溶液B变成溶液C时双氧水变成了水,是过氧化氢氧化亚铁离子为铁离子;
(4)固体B为C,C和浓硫酸加热反应生成二氧化碳、二氧化硫和水,结合化学方程式定量关系计算电子转移;
解答:
解:由Fe、CuO、C、Al组成的混合粉末加入过量氢氧化钠溶液过滤得到固体A为C、Fe、CuO,溶液A为NaAlO2,固体A加入过量稀硫酸过滤得到固体B为C,滤液B为FeSO4,CuSO4,加入过氧化氢氧化亚铁离子为铁离子;
(1)反应1是铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)反应2为铁和稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑,氧化铜和稀硫酸反应生成硫酸铜和水,反应的离子方程式为:
CuO+2H+=Cu2++H2O;
故答案为:Fe+2H+=Fe2++H2↑,CuO+2H+=Cu2++H2O;
(3)当溶液B变成溶液C时双氧水变成了水,是过氧化氢氧化亚铁离子为铁离子,结合电子守恒、原子守恒配平得到,反应的离子方程式为:2Fe2++1H2O2+2H+=2Fe3++2H2O,依据氧化还原反应中元素化合价变化,化合价升高的做还原剂,还原剂为Fe2+;
故答案为:2Fe2++1H2O2+2H+=2Fe3++2H2O;Fe2+;
(4)固体B为C,C和浓硫酸加热反应生成二氧化碳、二氧化硫和水,C+2H2SO4
CO2↑+2SO2↑+2H2O,结合化学方程式定量关系计算电子转移,2mol硫酸反应电子转移4mol,所以1.5mol硫酸反应电子转移3mol;
故答案为:3.
(1)反应1是铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)反应2为铁和稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑,氧化铜和稀硫酸反应生成硫酸铜和水,反应的离子方程式为:
CuO+2H+=Cu2++H2O;
故答案为:Fe+2H+=Fe2++H2↑,CuO+2H+=Cu2++H2O;
(3)当溶液B变成溶液C时双氧水变成了水,是过氧化氢氧化亚铁离子为铁离子,结合电子守恒、原子守恒配平得到,反应的离子方程式为:2Fe2++1H2O2+2H+=2Fe3++2H2O,依据氧化还原反应中元素化合价变化,化合价升高的做还原剂,还原剂为Fe2+;
故答案为:2Fe2++1H2O2+2H+=2Fe3++2H2O;Fe2+;
(4)固体B为C,C和浓硫酸加热反应生成二氧化碳、二氧化硫和水,C+2H2SO4
| ||
故答案为:3.
点评:本题考查了物质分离提纯的实验过程分析,物质性质的理解应用.化学方程式和离子方程式书写,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列各种描述中,正确的是( )
| A、氯水具有杀菌消毒作用,其中起作用的物质是氯气 |
| B、加碘食盐中所加的“碘”一般是碘化钾 |
| C、区别氯化铁溶液和氢氧化铁胶体可以用丁达尔效应 |
| D、用干燥的有色布条可以检验氯化氢气体中是否混有氯气 |
下列有关说法正确的是( )
| A、在同温同压下,相同体积的任何气体含有相同数目的原子 |
| B、氧化还原反应的判断依据是元素化合价是否有变化 |
| C、能导电的物质一定是电解质 |
| D、金属氧化物不一定是碱性氧化物 |
下列鉴别、分离或除杂方法中正确的是( )
| A、苯中含有少量苯酚,可用NaOH溶液除去 |
| B、NaOH固体中混有NH4HCO3,可直接加热除去NH4HCO3 |
| C、鉴别甲苯与己烯,可滴加酸性KMnO4溶液 |
| D、鉴别某溶液是否含有Fe2+,可先滴加新制氯水,再滴加KSCN溶液 |
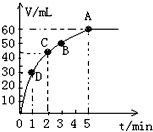 加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.(忽略溶液体积变化)
加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.(忽略溶液体积变化)