题目内容
下列属于电解质并能导电的物是( )
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤NaCl晶体 ⑥盐酸.
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤NaCl晶体 ⑥盐酸.
| A、① | B、①②③⑤⑥ |
| C、①②⑥ | D、①③④⑤ |
考点:电解质与非电解质
专题:
分析:电解质是在熔融状态或水溶液中能导电的化合物,电解质导电的条件有①熔融状态下②水溶液中,以此解答该题.
解答:
解:①NaCl为电解质,在熔融状态下能导电,故①正确;
②KNO3溶液能导电,但属于混合物,不是电解质,故②错误;
③Cu能导电,属于单质,既不是电解质也不是非电解质,故③错误;
④酒精是非电解质,故④错误;
⑤固体氯化钠在熔融状态下或水溶液中能够电离出阴阳离子,能够导电,属于电解质,氯化钠晶体中无自由移动的离子,不能导电,故⑤错误;
⑥盐酸能导电,盐酸属于混合物,既不是电解质也不是非电解质,故⑥错误.
故选A.
②KNO3溶液能导电,但属于混合物,不是电解质,故②错误;
③Cu能导电,属于单质,既不是电解质也不是非电解质,故③错误;
④酒精是非电解质,故④错误;
⑤固体氯化钠在熔融状态下或水溶液中能够电离出阴阳离子,能够导电,属于电解质,氯化钠晶体中无自由移动的离子,不能导电,故⑤错误;
⑥盐酸能导电,盐酸属于混合物,既不是电解质也不是非电解质,故⑥错误.
故选A.
点评:本题考查电解质的电离和电解质的概念,题目难度不大,注意电解质、非电解质的区别,本题注意一下几点:①混合物和单质既不是电解质也不是非电解质;②电解质不一定导电.

练习册系列答案
相关题目
下列有关说法正确的是( )
| A、在同温同压下,相同体积的任何气体含有相同数目的原子 |
| B、氧化还原反应的判断依据是元素化合价是否有变化 |
| C、能导电的物质一定是电解质 |
| D、金属氧化物不一定是碱性氧化物 |
现有A.B.C三种化合物,各取20g相混合,完全反应后,得9g B,24.5g C,还有D生成.已知D的相对分子质量为106.现将11gA和5.5gB反应,能生成D( )
| A、1mol |
| B、0.5mol |
| C、0.125mol |
| D、0.25mol |
下列有关叙述正确的是( )
| A、任何晶体中,若含有阳离子也一定含有阴离子 |
| B、金属键越强,则该金属的金属性越强 |
| C、金属钨的熔点高于金属钠,是因为钨的金属键更强 |
| D、金属导电的过程实质上就是金属键被破坏的过程,不能用“电子气理论”来解释 |

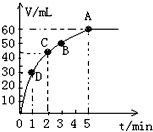 加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.(忽略溶液体积变化)
加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.(忽略溶液体积变化)