题目内容
将气体A2和B2各1mol注入容积为1L的密闭容器中反应生成C,平衡时测得c(A2)=0.58mol/L,则c(B2)=0.16mol/L,c(C)=0.84mol/L,则C的分子式为( )
| A、AB2 |
| B、A2B4 |
| C、AB |
| D、A2B |
考点:化学平衡的计算
专题:化学平衡专题
分析:根据平衡时反应物和生成物的浓度求算出反应物和生成物的物质的量变化量之比,写出反应方程式,根据原子守恒写出C的分子式.
解答:
解:开始A2和B2两种气体的浓度均为1mol/L,在密闭容器内反应生成气体C,达平衡后,测得:c(A2)=0.58mol/L,c(B2)=0.16mol/L,c(C)=0.84mol/L,
故△c(A2)=1mol/L-0.58mol/L=0.42mol/L,
△c(B2)=1mol/L-0.16mol/L=0.84mol/L,
△c(C)=0.84mol/L,
故A2、B2、C的化学计量数之比为0.42mol/L:0.84mol/L:0.84mol/L=1:2:2,
故该反应可表示为A2+2B2?2C,根据原子守恒可知,C为AB2.
故选:A.
故△c(A2)=1mol/L-0.58mol/L=0.42mol/L,
△c(B2)=1mol/L-0.16mol/L=0.84mol/L,
△c(C)=0.84mol/L,
故A2、B2、C的化学计量数之比为0.42mol/L:0.84mol/L:0.84mol/L=1:2:2,
故该反应可表示为A2+2B2?2C,根据原子守恒可知,C为AB2.
故选:A.
点评:本题考查了化学平衡的相关计算,根据原子守恒写出C的分子式是解题的关键.

练习册系列答案
相关题目
下列有关实验原理或实验操作正确的是( )
A、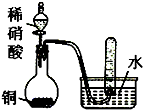 验证铜与稀硝酸的反应产物是NO |
B、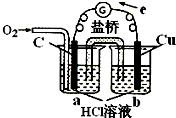 实现化学反应:2Cu+O2+4H+=2Cu2++2H2O |
C、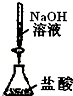 测定盐酸的浓度 |
D、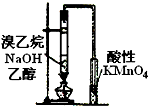 检验溴乙烷与NaOH醇溶液共热有乙烯生成 |
分离下列三组混合物依次采取的方法正确的是:①植物油和氯化钠溶液 ②碳酸钙和氯化钙的水溶液 ⑧氯化钠和碘( )
| A、分液、蒸馏、萃取 |
| B、蒸发、过滤、分液 |
| C、分液、过滤、加热升华 |
| D、蒸馏、萃取、分液 |
将铁的化合物溶于盐酸,滴加KSCN溶液,不发生颜色变化,再加入适量氯水,溶液立即呈红色的是( )
| A、Fe2O3 |
| B、FeCl3 |
| C、Fe2(SO4)3 |
| D、FeO |
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq) 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq) 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )| A、反应I2(aq)+I-(aq)?I3-(aq)的△H>0 |
| B、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C、若反应进行到状态D时,平衡向逆反应方向移动 |
| D、状态B与状态C相比,状态C的c(I2)大 |
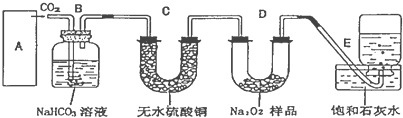
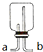 可连接在E处,则Cl2从
可连接在E处,则Cl2从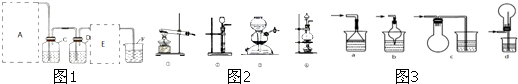
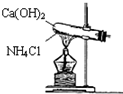 实验室通常用如图所示的装置来制取氨气,(收集装置略).回答下列问题:
实验室通常用如图所示的装置来制取氨气,(收集装置略).回答下列问题: