题目内容
过氧化钠在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
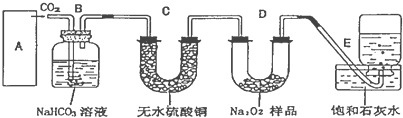
(1)过氧化钠与二氧化碳反应的化学方程式为: .
(2)A是制取CO2的装置,C装置内可能出现的现象是 ,为了检验E中收集到的气体,采取的操作方法是 .
(3)判断D中的1.95g过氧化钠样品是否反应完毕是通过观察E装置中的现象来完成的,你预测样品反应完毕时E装置内有何现象?
、 .
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值小约 mL(所用数据均在标准状况下测定),可能的原因是 .
(5)将16.8g CO2和H2O的混合气体,通入足量的Na2O2中,可得O2在标准状况下为5.6L,则原混合气体中CO2与H2O的物质的量之比为 .

(1)过氧化钠与二氧化碳反应的化学方程式为:
(2)A是制取CO2的装置,C装置内可能出现的现象是
(3)判断D中的1.95g过氧化钠样品是否反应完毕是通过观察E装置中的现象来完成的,你预测样品反应完毕时E装置内有何现象?
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值小约
(5)将16.8g CO2和H2O的混合气体,通入足量的Na2O2中,可得O2在标准状况下为5.6L,则原混合气体中CO2与H2O的物质的量之比为
考点:碱金属及其化合物的性质实验,常见气体制备原理及装置选择
专题:实验设计题
分析:(1)过氧化钠和二氧化碳反应生成碳酸钠和氧气,注意该反应中过氧化钠既是氧化剂又是还原剂;
(2)无水硫酸铜吸水后变成蓝色晶体;使带火星的木条复燃的气体是氧气;
(3)根据装置内气体的压强判断现象;
(4)根据过氧化钠的质量可以生成氧气的体积,理论生成气体的体积-实际氧气的体积=差值;
(5)根据n=
计算氧气物质的量,由2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2,可知二氧化碳和水蒸气都是2mol反应生成1mol氧气,可计算混合气体总物质的量,设CO2物质的量为xmol,水蒸气物质的量为(0.3-x)mol,利用二者质量列方程计算.
(2)无水硫酸铜吸水后变成蓝色晶体;使带火星的木条复燃的气体是氧气;
(3)根据装置内气体的压强判断现象;
(4)根据过氧化钠的质量可以生成氧气的体积,理论生成气体的体积-实际氧气的体积=差值;
(5)根据n=
| V |
| Vm |
解答:
解:(1)过氧化钠和二氧化碳反应生成碳酸钠和氧气,故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(2)无水硫酸铜吸水后变成蓝色晶体CuSO4?H2O,过氧化钠和二氧化碳反应生成氧气,氧气能使带火星的木条复燃,
故答案为:白色固体变蓝;取下集气瓶,竖立起来,用带余烬木条深入瓶内,观察木条是否复燃;
(3)当D中的1.95g过氧化钠样品接近反应完毕时,由于生成氧气的量减少,压强变小,所以E中可能会因二氧化碳与石灰水反应而倒吸.
故答案为:由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸;
(4)1.95g过氧化钠完全反应生成氧气的体积为v.
2Na2O2----O2;
2mol 22.4L
v
v=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小.
280mL-250mL=30mL;
原因是Na2O2可能含有其它杂质,
故答案为:30;Na2O2可能含有其它杂质;
(5)生成氧气物质的量=
=0.25mol,
由2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2,可知二氧化碳和水蒸气都是2mol反应生成1mol氧气,故混合气体物质的量为0.25mol×2=0.5mol,设CO2物质的量为xmol,水蒸气物质的量为(0.5-x)mol,则:
44x+(0.5-x)×18=16.8;
解得:x=0.3mol,
所以水的物质的量=0.5mol-0.3mol=0.2mol,
原混合气体中CO2与H2O的物质的量之比为3:2,故答案为3:2.
(2)无水硫酸铜吸水后变成蓝色晶体CuSO4?H2O,过氧化钠和二氧化碳反应生成氧气,氧气能使带火星的木条复燃,
故答案为:白色固体变蓝;取下集气瓶,竖立起来,用带余烬木条深入瓶内,观察木条是否复燃;
(3)当D中的1.95g过氧化钠样品接近反应完毕时,由于生成氧气的量减少,压强变小,所以E中可能会因二氧化碳与石灰水反应而倒吸.
故答案为:由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸;
(4)1.95g过氧化钠完全反应生成氧气的体积为v.
2Na2O2----O2;
2mol 22.4L
| 1.95g |
| 78g/mol |
v=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小.
280mL-250mL=30mL;
原因是Na2O2可能含有其它杂质,
故答案为:30;Na2O2可能含有其它杂质;
(5)生成氧气物质的量=
| 5.6L |
| 22.4L/mol |
由2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2,可知二氧化碳和水蒸气都是2mol反应生成1mol氧气,故混合气体物质的量为0.25mol×2=0.5mol,设CO2物质的量为xmol,水蒸气物质的量为(0.5-x)mol,则:
44x+(0.5-x)×18=16.8;
解得:x=0.3mol,
所以水的物质的量=0.5mol-0.3mol=0.2mol,
原混合气体中CO2与H2O的物质的量之比为3:2,故答案为3:2.
点评:本题考查了钠及其化合物的性质,难度不大,注意过氧化钠和二氧化碳反应中过氧化钠既是氧化剂又是还原剂.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36,K1(H2S)=1.3×10-20. 向0.10mol?L-1Fe2+和0.10mol?L-1Cu2+的混合溶液中通入H2S气体至饱和(c(H2S) 0.10mol?L-1).请推断沉淀生成情况是下列哪一种( )
| A、先生成CuS 沉淀,后生成FeS 沉淀 |
| B、先生成FeS 沉淀,后生成CuS 沉淀 |
| C、先生成CuS 沉淀,不生成FeS 沉淀 |
| D、先生成CuS 沉淀,反应一段时间FeS和CuS同时沉淀 |

 工业上以黄铁矿为原料,采用接触法生产硫酸.请回答下列问题:
工业上以黄铁矿为原料,采用接触法生产硫酸.请回答下列问题:
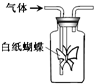 如图集气瓶中用滤纸折成的纸蝴蝶上喷洒了一种溶液,通入某种气体后,实验结果与预测的纸蝴蝶颜色变化不一致的是( )
如图集气瓶中用滤纸折成的纸蝴蝶上喷洒了一种溶液,通入某种气体后,实验结果与预测的纸蝴蝶颜色变化不一致的是( )