题目内容
1.能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的开发是当今社会人类面临的严峻课题.回答下列问题:(1)我国是世界上少数以煤为主要燃料的国家,下列关于煤作燃料的论点正确的是ACD.
A.煤是重要的化工原料,把煤作燃料简单燃烧掉太可惜,应该综合利用
B.煤是发热很高的固体燃料,我国煤炭资源相对集中,开采成本低,用煤作燃料合算
C.煤燃烧时产生大量二氧化硫和烟尘,对环境污染严重
D.通过洁净煤技术,如煤的气化和液化以及烟气脱硫,不仅减轻了燃煤污染,还能提高煤燃烧的热利用率
(2)乌克兰科学家将铜和铁混合熔化制成多孔金属,用于制作太空火箭上使用的煤油燃料雾化器,该雾化器的作用是增大接触面积,使燃料燃烧更充分.
分析 (1)煤可燃烧,燃烧时产生大量二氧化硫和烟尘,且燃烧效率较低,可通过洁净煤技术,如煤的气化和液化以及烟气脱硫,提高煤燃烧的热利用率;
(2)多孔金属具有较大的接触面积.
解答 解:(1)煤可燃烧,燃烧时产生大量二氧化硫和烟尘,且燃烧效率较低,可通过洁净煤技术,如煤的气化和液化以及烟气脱硫,提高煤燃烧的热利用率,如用煤直接做燃料,可导致环境污染,造成较大浪费,ACD正确,
故答案为:ACD;
(2)物质气态时燃烧时更充分,故煤油燃料雾化器能将煤油由液态雾化为气态,燃烧更充分,故答案为:增大接触面积,使燃料燃烧更充分.
点评 本题考查环境污染问题,能源、信息、材料、环境是当今世界四大首要问题,在能源危机日趋严重的今天,它既是社会热点,也是化学考查的热点,主要侧重能源的分类、能源使用对环境的影响、新能源开发的技术和前景等.

练习册系列答案
相关题目
3. 乙苯催化脱氢生产苯乙烯的反应:
乙苯催化脱氢生产苯乙烯的反应: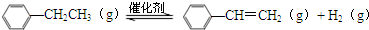
(1)已知:
计算上述反应的△H=+124 kJ•mol-1.
(2)一定温度下,将a mol乙苯加入体积为V L的密闭容器中,发生上述反应,反应时间与容器内气体总压强的数据如下表.
①平衡时,容器中气体物质的量总和为1.4amol,乙苯的转化率为40%.
②计算此温度下该反应的平衡常数K$\frac{4a}{15V}$.
(3)实际生产时反应在常压下进行,且向乙苯蒸气中掺入水蒸气,利用热力学数据计算得到温度和投料比M对乙苯平衡转化率的影响可用右图表示.[M=n(H2O)/n(乙苯)]
①比较图中A、B两点对应的平衡常数大小:KA<KB
②图中投料比(M1、M2、M3)的大小顺序为M1>M2>M3.
③某研究机构用CO2代替水蒸气开发了绿色化学合成工艺--乙苯-二氧化碳耦合催化脱氢制苯乙烯.保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO.新工艺的特点有①②③④(填编号).
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利于CO2资源利用.
 乙苯催化脱氢生产苯乙烯的反应:
乙苯催化脱氢生产苯乙烯的反应: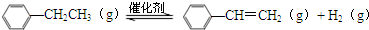
(1)已知:
化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | 612 | 436 |
(2)一定温度下,将a mol乙苯加入体积为V L的密闭容器中,发生上述反应,反应时间与容器内气体总压强的数据如下表.
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| 总压强/100kPa | 1.0 | 1.2 | 1.3 | 1.4 | 1.4 |
②计算此温度下该反应的平衡常数K$\frac{4a}{15V}$.
(3)实际生产时反应在常压下进行,且向乙苯蒸气中掺入水蒸气,利用热力学数据计算得到温度和投料比M对乙苯平衡转化率的影响可用右图表示.[M=n(H2O)/n(乙苯)]
①比较图中A、B两点对应的平衡常数大小:KA<KB
②图中投料比(M1、M2、M3)的大小顺序为M1>M2>M3.
③某研究机构用CO2代替水蒸气开发了绿色化学合成工艺--乙苯-二氧化碳耦合催化脱氢制苯乙烯.保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO.新工艺的特点有①②③④(填编号).
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利于CO2资源利用.
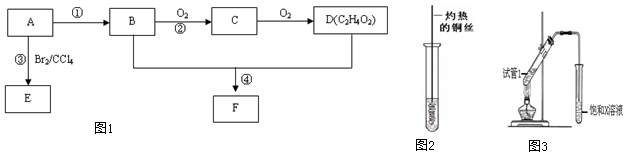
 ;
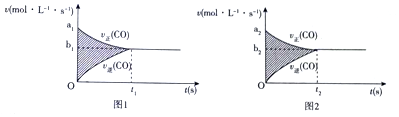
;

 .
.