题目内容
13.某气态烃A在标准状况下的密度为1.25g/L,其产量可以用来衡量一个国家的石油化工发展水平.B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,F有香味.它们之间的转化关系如图1所示: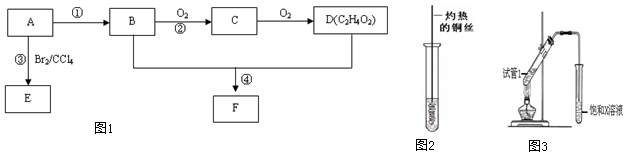
(1)B的结构简式为CH3CH2OH,D中官能团的名称为羧基.
(2)反应①的反应类型是加成反应,反应③的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图2所示).重复操作2-3次.该反应的化学方程式为2CH3CH2OH+O2$\stackrel{△}{→}$2CH3CHO+2H2O.
(4)B、D在浓硫酸的作用下实现反应④,实验装置如图3所示:试管1中装入药品和碎瓷片后加热.
①碎瓷片的作用是防暴沸.
②图中X的化学式为Na2CO3.其作用是溶解乙醇、吸收乙酸、减少乙酸乙酯的溶解度,有利于乙酸乙酯分层.
③试管1反应的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
分析 A是一种气态烃,在标准状况下的密度是1.25g/L,摩尔质量=1.25g/L×22.4L/mol=28g/mol,其产量是衡量一个国家石油化工发展水平,则A为CH2=CH2;B氧化生成C、C氧化生成D,B和D都是生活中常见的有机物,结合D的分子式可知,B为CH3CH2OH,C为CH3CHO,D为CH3COOH,故反应①是乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH和CH3COOH在浓硫酸作用下发生酯化反应生成F为CH3COOCH2CH3,乙烯与溴发生加成反应生成E为CH2BrCH2Br.
解答 解:A是一种气态烃,在标准状况下的密度是1.25g/L,摩尔质量=1.25g/L×22.4L/mol=28g/mol,其产量是衡量一个国家石油化工发展水平,则A为CH2=CH2;B氧化生成C、C氧化生成D,B和D都是生活中常见的有机物,结合D的分子式可知,B为CH3CH2OH,C为CH3CHO,D为CH3COOH,故反应①是乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH和CH3COOH在浓硫酸作用下发生酯化反应生成F为CH3COOCH2CH3,乙烯与溴发生加成反应生成E为CH2BrCH2Br,
(1)B的结构简式为CH3CH2OH,D为CH3COOH,官能团名称是羧基,
故答案为:CH3CH2OH;羧基;
(2)反应①的反应类型是加成反应,反应③是乙烯与溴发生加成反应生成1,2-二溴乙烷,反应方程式为:CH2=CH2+Br2→CH2BrCH2Br,
故答案为:加成反应;CH2=CH2+Br2→CH2BrCH2Br;
(3)该反应为乙醇的催化氧化,该反应化学方程式为2CH3CH2OH+O2$\stackrel{△}{→}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$\stackrel{△}{→}$2CH3CHO+2H2O;
(4)B、D在浓硫酸的作用下实现反应④,实验装置如图3所示:试管1中装入药品和碎瓷片后加热.
①碎瓷片的作用是防暴沸,防止产生安全事故,故答案为:防暴沸;
②图中X的化学式为Na2CO3,饱和碳酸钠溶液能溶解乙醇、吸收乙酸、减少乙酸乙酯的溶解度,有利于乙酸乙酯分层,
故答案为:Na2CO3;溶解乙醇、吸收乙酸、减少乙酸乙酯的溶解度,有利于乙酸乙酯分层;
③试管1反应为乙酸、乙醇的酯化反应,该反应的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$ CH3COOCH2CH3+H2O,
故答案为:CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$ CH3COOCH2CH3+H2O.
点评 本题考查有机物的推断,为高频考点,涉及烯、醇、醛、羧酸等的性质与转化等,正确推断物质是解本题关键,注意乙酸乙酯制取中饱和碳酸钠溶液的作用,题目难度不大.

 期末集结号系列答案
期末集结号系列答案| A. | 1s22s22p63s23p63d104s1 | B. | 1s22s22p63s23p63d64s2 | ||
| C. | 1s22s22p63s23p63d34s2 | D. | 1s22s22p63s23p63d44s2 |
| A. | 相等 | B. | 后者是前者的11倍 | ||
| C. | 后者是前者的108 | D. | 前者是后者的108 |
| A. | O2的摩尔质量是32g | B. | 氯化钠的相对原子质量是58.5g | ||
| C. | 1molH2O的质量是18g | D. | 1molH2O含有氢原子的个数2个 |
| A. | 使用催化剂,可加快反应速率,目的是提高生产效率 | |
| B. | 使用冰箱保存食物,是利用了化学反应速率理论 | |
| C. | 化学反应速率理论是研究怎样提高原料转化率 | |
| D. | 化学平衡理论是研究怎样使用有限原料多出产品 |
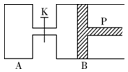 图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入1mol X、1mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达平衡时,VB=0.6a L.回答下列问题:
图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入1mol X、1mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达平衡时,VB=0.6a L.回答下列问题: