题目内容
16.X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,Y的电负性在同周期中最大,Z的离子半径在同周期中最小,下列关于X、Y、Z叙述中不正确的是( )| A. | 元素X与元素Y能形成离子化合物 | |
| B. | 原子序数为:X<Y<Z | |
| C. | 元素Z最高价氧化物对应水化物具有两性 | |
| D. | 元素Y形成的气态氢化物水溶液呈强酸性 |
分析 X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,X为Na元素;Y的电负性在同周期中最大,Y为Cl元素;Z的离子半径在同周期中最小,Z为Al元素,据此结合元素周期律与物质的性质解答.
解答 解:X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,X为Na元素,Y的电负性在同周期中最大,Y为Cl元素,Z的离子半径在同周期中最小,Z为Al元素,
A.X为Na、Y为Cl元素,二者能够形成离子化合物是NaCl,故A正确;
B.原子序数Na<Al<Cl,同周期随原子序数增大,原子半径减小,原子半径Na>Al>Cl,故B错误;
C.Z为Al元素,其最高价氧化物对应水化物为氢氧化铝,氢氧化铝是两性氢氧化物,既能与强酸反应,又能与强碱反应,故C正确;
D.Y为Cl元素,其气态氢化物是HCl,HCl溶于水得到盐酸,盐酸呈强酸性,故D正确;
故选B.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,推断元素为解答关键,注意掌握原子结构与元素周期表、元素周期律的关系,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
7.下列括号内有关物质的描述及用途错误的是( )
| A. | 硅(半导体材料) | B. | 二氧化硅(制光导纤维) | ||
| C. | Na2Si03 (用作粘合剂,俗称水玻璃) | D. | Al(OH)3(用作胃药,俗称人造刚玉) |
4.某实验兴趣小组按如图装置实验后,所记录内容合理的是( ) 

实验 记录 | ①Zn质量减少,Cu质量不变; ②外电路电流方向是:由Cu→Zn; ③SO42- 向Cu极移动; ④Zn电极发生氧化反应; ⑤正极反应式:Cu2++2e-═Cu |
| A. | ①②④ | B. | ②③④ | C. | ②④⑤ | D. | ①③⑤ |
11.下列实验中,所使用的装置(夹持装置略)、试剂和操作方法都正确的是( )
| A. | 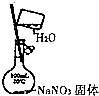 配置一定物质的量 浓度的NaNO3溶液 | |
| B. | 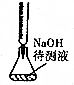 中和滴定 | |
| C. | 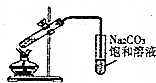 制备乙酸乙酯 | |
| D. | 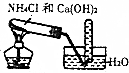 实验室制取氨 |
1.下列互为同位素的是( )
| A. | 2412Mg和2612Mg | B. | O2和O3 | C. | NO和NO2 | D. | H2O和H2O2 |
8.根据元素周期律进行推断,下列不正确的是( )
| A. | 碱性:KOH>NaOH | B. | Mg、Al与同浓度盐酸反应,Mg更剧烈 | ||
| C. | 稳定性:HBr>HI | D. | 酸性:H3PO4>HNO3 |
5.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A. | 粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-═Cu2+ | |
| B. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | |
| C. | 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-═Cl2↑ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
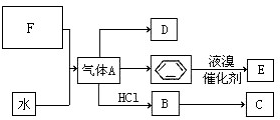 已知:C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空:
已知:C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空: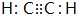 ;C的结构简式
;C的结构简式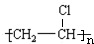 ;
; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反应类型为取代反应;
+HBr,其反应类型为取代反应;