��Ŀ����
4�� �״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ش��������⣺
�״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ش��������⣺��1��һ���¶��£���һ���ݵ��ܱ������У���CO��H2�ϳɼ״���CO��g��+2H2��g��?CH3OH��g��
���������β���˵���÷�Ӧ�Ѵﵽƽ��״̬����C������ţ���
A��ÿ����1mol CO��ͬʱ����2molH2
B��������������ʵ�������
C������CH3OH������������CO���������
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��CO��ƽ��ת���ʣ��������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��B��C�����ƽ�ⳣ��K��B����K��C�� �����������=����������
��ij�¶��£���2.0mol CO��6.0molH2����2L���ܱ������У��ﵽƽ��ʱ���c��CO��=0.25mol/L��CO��ת����=75%�����¶��µ�ƽ�ⳣ��K=1.3��������λ��Ч���֣���
��2�������£���VmL��0.20mol/L����������Һ��μ��뵽20.00mL��0.20mol/L������Һ�У���ַ�Ӧ����ҺpH=7����ʱV��20.00�����������=����������������������Һ�������Һǡ����ȫ��Ӧʱ����Һ����������Ũ���ɴ�С����˳��c��Na+����c��HCOO-����c��OH-����c��H+����
��3���¶�650���������ȼ�ϵ�أ��ã�CO��H2������Ӧ�������CO2�Ļ������Ϊ������Ӧ������缫����Li2CO3��Na2CO3�����������ʣ��õ�ص�������ӦʽΪO2+4e-+2CO2�T2CO32-��
��4����֪��CH3OH��H2��ȼ���ȣ���H���ֱ�Ϊ-726.5kJ/mol��-285.8kJ/mol��������CO2��H2��Ӧ����CH3OH��H2O���Ȼ�ѧ����ʽ��CO2��g��+3H2��g���TCH3OH��l��+H2O��l����H=-130.9 kJ/mol��
���� ��1���ٵ��ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��ٸı䣬�ɴ�������һЩ���������䣬���Դ��ж��Ƿ�õ�ƽ��״̬��
����5.0MPaʱ�������¶����ߣ�COת���ʼ�С��ƽ�����ƣ�
�۸��ݻ�ѧ��Ӧ����ʽ������ת���ʣ���ƽ�ⳣ��K=$\frac{c��C{H}_{3}OH��}{c��CO��•{c}^{2}��{H}_{2}��}$���㣻
��2����Һ��������Ǹ�����Һ��H+Ũ����OH-Ũ�ȵ���Դ�С�жϵģ�ֻҪ��Һ��c��H+��=c��OH-������Һ�ͳ����ԣ�HCOOH��������ʣ�����̶Ȳ���NaOH��ǿ����ʣ���ȫ���룬��Ӧ���ɵļ�������ǿ��������ˮ��ʼ��ԣ�����Һ�����ԣ����ټӼ������������Һ�������Һǡ����ȫ��Ӧʱ����Һ�Լ��ԣ����������ˮ��Ũ�ȼ�С��
��3�������������õ��ӺͶ�����̼��Ӧ����̼������Ӷ�������ԭ��Ӧ��
��4������ȼ���ȵĸ����Լ���˹���������㻯ѧ��Ӧ���ʱ䣬Ȼ��д���Ȼ�ѧ����ʽ��
��� �⣺��1����A��ÿ����1mol COΪ�����ʣ�����2molH2Ϊ�����ʣ���������֮�ȵ��ڼ�����֮�ȣ�˵���÷�Ӧ�ﵽƽ��״̬������ȷ��
B����Ӧ������������ʵ������٣���������������ʵ������䣬��˵���÷�Ӧ�ﵽƽ��״̬������ȷ��
C������CH3OH������Ϊ�����ʣ�����CO������Ϊ�����ʣ�ͬΪ�����ʲ���˵���Ƿ�ﵽƽ��״̬���ʴ���
D�����ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��ٸı䣬��Ӧ���ﵽƽ��״̬������CH3OH��CO��H2��Ũ�ȶ����ٷ����仯��˵���÷�Ӧ�ﵽƽ��״̬������ȷ��
�ʴ�Ϊ��C��
����5.0MPaʱ�������¶����ߣ�COת���ʼ�С��ƽ�����ƣ���ƽ�ⳣ����С���������¶�����K��С������K��B����K��C����
�ʴ�Ϊ������
�۽�2.0mol CO��6.0mol H2����2L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c��CO��=0.25mol/L����
CO��g��+2H2��g���TCH3OH��g��
��ʼŨ�ȣ�1.0 3.0 0
�仯Ũ�ȣ�0.75 1.5 0.75
ƽ��Ũ�ȣ�0.25 1.5 0.75
CO��ת����$\frac{0.75}{1}$��100%=75%�����¶��µĻ�ѧƽ�ⳣ��K=$\frac{c��C{H}_{3}OH��}{c��CO��•{c}^{2}��{H}_{2}��}$=$\frac{0.75}{0.25��1��{5}^{2}}$��1.3��
�ʴ�Ϊ��75%��1.3��
��2��CH3COOH��������ʣ�����̶Ȳ���NaOH��ǿ����ʣ���ȫ���룬��Ӧ���ɵļ�������ǿ�������Σ�ˮ��ʼ��ԣ�����Һ������pH=7�����ټӼ���Գ����£���V mL��0.20mol•L-1����������Һ��μ��뵽20.00mL��0.20mol•L-1������Һ�У���ַ�Ӧ��V��20.00mL��Һ������pH=7��c��H+��=c��OH-����������������Һ�������Һǡ����ȫ��Ӧʱ����Һ�Լ��ԣ����������ˮ��Ũ�ȼ�С����Һ������Ũ�ȴ�С��ϵΪ��c��Na+����c��HCOO-����c��OH-����c��H+����
�ʴ�Ϊ������c��Na+����c��HCOO-����c��OH-����c��H+����
��3�������������õ��ӺͶ�����̼��Ӧ����̼������Ӷ�������ԭ��Ӧ���缫��ӦʽΪ��O2+4e-+2CO2=2CO32-��
�ʴ�Ϊ��O2+4e-+2CO2=2CO32-��
��4����H2��g����ȼ���ȡ�HΪ-285.8kJ•mol-1֪��1molH2��g����ȫȼ������1molH2O��l���ų�����285.8kJ��
����H2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-285.8kJ•mol-1��
��CH3OH��l��+$\frac{1}{2}$O2��g��=CO2��g��+2 H2O��l����H=-726.5kJ•mol-1��
�ɸ�˹���ɿ�֪��3����-�ڵ�CO2��g��+3H2��g��=CH3OH��l��+H2O��l����H=-130.9 kJ•mol-1��
�ʴ�Ϊ��CO2��g��+3H2��g��=CH3OH��l��+H2O��l����H=-130.9 kJ•mol-1��
���� ���⿼���˻�ѧƽ��״̬���жϡ���ѧƽ���ƶ��Լ���ѧƽ�ⳣ��������Ũ�ȴ�С�Ƚϡ��缫����ʽ����д���Ȼ�ѧ����ʽ����д�ȣ���Ŀ�漰��֪ʶ��϶࣬�����ڿ���ѧ���Ի���֪ʶ���ۺ�Ӧ����������Ŀ�Ѷ��еȣ�

 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д�| A�� | ����H2O�����е����������ڷ�Ӧ��H2��O2�����е������� | |
| B�� | ��Ӧ��H2��O2�����е����������ڲ���H2O�����е������� | |
| C�� | ��Ӧ��H2��O2�����е����������ڲ���H2O�����е������� | |
| D�� | ��Ӧ��H2��O2�����е������������H2O�����е�������֮��û��ֱ�ӹ�ϵ |
| A�� | һ������ĽṹʽCH3Cl | |
| B�� | ����Ľṹ��ʽCH3��CH2��2CH3 | |
| C�� | �Ȼ�����ӵ��γɹ��̿��õ���ʽ��ʾΪ�� | |
| D�� | ���Ȼ�̼�ĵ���ʽ |
| A�� | ��ˮ���ú�pH���� | |
| B�� | Na�Ľ����Ա�Mgǿ���ʿ���Na��MgCl2��Һ��Ӧ��ȡMg | |
| C�� | Ũ�����е�HNO3�����ֽ⣬����ʱ��ʵ���ҿ�����Ũ����ʻ�ɫ | |
| D�� | ���ó���ʯ��ˮ��ȥCO2�л��е�����SO2 |
| A�� | ��������������ˮ�У��и�ʱҪ��ˮ�½��� | |
| B�� | Һ��ֱ�ӱ�����ĥ�ڲ�������ϸ����ɫƿ�� | |
| C�� | KOH��Һ�����ĥ�ڲ������Ĺ��ƿ�� | |
| D�� | ���������ƴ������ˮ�Ҵ��� |
| A�� | ��ϩ�;���ϩ����ʹ����KMnO4��Һ��ɫ | |
| B�� | ����������ϩ�����ϩ��ȫȼ�գ�������CO2������� | |
| C�� | �Ҵ������ѣ�CH3CH2OCH2CH3����Ϊͬ���칹�� | |
| D�� | ��Ȳ�뱽��Ϊͬϵ�� |
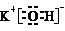 ����O2�ĽṹʽO=O����K2FeO4��Fe�Ļ��ϼ�Ϊ+6����������Ӧ�����ӷ���ʽ4FeO42-+10H2O=4Fe��OH��3�����壩+3O2��+8OH-��
����O2�ĽṹʽO=O����K2FeO4��Fe�Ļ��ϼ�Ϊ+6����������Ӧ�����ӷ���ʽ4FeO42-+10H2O=4Fe��OH��3�����壩+3O2��+8OH-��
 $\stackrel{KOH}{��}$H-C��
$\stackrel{KOH}{��}$H-C��
 +H2O��-R��-R�䡢-R���ʾ���ظ���̬����ܲ�ͬ��ԭ�ӻ�ԭ���ţ�
+H2O��-R��-R�䡢-R���ʾ���ظ���̬����ܲ�ͬ��ԭ�ӻ�ԭ���ţ� ����Ӧ�����Ǽӳɷ�Ӧ��
����Ӧ�����Ǽӳɷ�Ӧ�� ��
�� ��
�� ��
��

 ��
�� ��
��