题目内容
有A、B、C、D四种短周期的主族元素,原子序数依次增大,其原子的最外层电子数依次为4、3、6、7.A原子的次外层有2个电子,B、C、D原子的次外层都为8个电子.
(1)写出元素名称:A 、B 、C 、D
(2)以上某元素的单质可用于制造漂白粉,请写出制取漂白粉的化学方程式 .
(1)写出元素名称:A
(2)以上某元素的单质可用于制造漂白粉,请写出制取漂白粉的化学方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:有A、B、C、D四种短周期的主族元素,原子序数依次增大,其原子的最外层电子数依次为4、3、6、7,A原子的次外层有2个电子,最外层电子数不能超过8个,所以A原子的次外层是K层,则A为C元素,B、C、D原子的次外层都为8个电子,则B、C、D位于第三周期,B元素的最外层电子数为3且原子序数大于A,则B是Al元素、C是S元素、D是Cl元素,再结合物质的性质分析解答.
解答:
解:有A、B、C、D四种短周期的主族元素,原子序数依次增大,其原子的最外层电子数依次为4、3、6、7,A原子的次外层有2个电子,最外层电子数不能超过8个,所以A原子的次外层是K层,则A为C元素,B、C、D原子的次外层都为8个电子,则B、C、D位于第三周期,B元素的最外层电子数为3且原子序数大于A,则B是Al元素、C是S元素、D是Cl元素,
(1)通过以上分析知,A、B、C、D元素名称分别是碳、铝、硫、氯,故答案为:碳;铝;硫;氯;
(2)氯气和氢氧化钙溶液制取漂白粉,反应方程式为:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,故答案为:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
(1)通过以上分析知,A、B、C、D元素名称分别是碳、铝、硫、氯,故答案为:碳;铝;硫;氯;
(2)氯气和氢氧化钙溶液制取漂白粉,反应方程式为:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,故答案为:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
点评:本题考查了元素位置结构性质的相互关系及应用,熟悉原子结构、元素周期表中元素位置关系是解本题关键,熟记元素周期表中前36号元素,知道漂白粉的制取原理,明确漂白粉的有效成分与主要成分的区别,题目难度不大.

练习册系列答案
相关题目
下列物质转化需要加入还原剂才能实现的是( )
| A、SO32-→SO2 |
| B、HCl→Cl2 |
| C、Na→Na+ |
| D、NO→N2 |
下列各装置中,能够成原电池的是( )
A、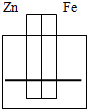 乙醇 |
B、 稀硫酸 |
C、 稀硫酸 |
D、 稀硫酸 稀硫酸 |

 和HOCH2CH2OH两种单体可通过
和HOCH2CH2OH两种单体可通过
 【化学反应原理(选修4)】
【化学反应原理(选修4)】