题目内容
下列实验操作中,溶液里无固体析出的是( )
| A、MgCl2溶液中加入Na的小颗粒 |
| B、Ca(OH)2饱和溶液中加入Na的小颗粒 |
| C、KHCO3稀溶液中加入Na的小颗粒 |
| D、Ca(HCO3)2溶液中加入一小块钠 |
考点:钠的化学性质
专题:金属概论与碱元素
分析:钠和水反应生成氢氧化钠和氢气,
A.氢氧化钠和氯化镁发生复分解反应;
B.溶剂的质量减少,导致溶液成为过饱和溶液;
C.碳酸氢钾和氢氧化钠发生复分解反应;
D.氢氧化钠和碳酸氢钙发生复分解反应.
A.氢氧化钠和氯化镁发生复分解反应;
B.溶剂的质量减少,导致溶液成为过饱和溶液;
C.碳酸氢钾和氢氧化钠发生复分解反应;
D.氢氧化钠和碳酸氢钙发生复分解反应.
解答:
解:钠和水反应生成氢氧化钠和氢气,
A.氢氧化钠和氯化镁发生反应生成氢氧化镁沉淀和氯化钠,故A错误;
B.溶剂的质量减少,导致溶液成为过饱和溶液,会析出部分氢氧化钙固体,故B错误;
C.碳酸氢钾和氢氧化钠发生反应生成可溶性的碳酸钠和碳酸钾,所以没有固体析出,故C正确;
D.氢氧化钠和碳酸氢钙发生反应生成难溶性的碳酸钙沉淀,所以析出固体,故D错误;
故选C.
A.氢氧化钠和氯化镁发生反应生成氢氧化镁沉淀和氯化钠,故A错误;
B.溶剂的质量减少,导致溶液成为过饱和溶液,会析出部分氢氧化钙固体,故B错误;
C.碳酸氢钾和氢氧化钠发生反应生成可溶性的碳酸钠和碳酸钾,所以没有固体析出,故C正确;
D.氢氧化钠和碳酸氢钙发生反应生成难溶性的碳酸钙沉淀,所以析出固体,故D错误;
故选C.
点评:本题考查了物质间的反应,明确物质的性质是解本题关键,结合物质的溶解性、溶解度来分析解答即可,难度不大.

练习册系列答案
相关题目
取100mL 2mol/L和300mL 1mol/L的硫酸注入500mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是( )
| A、1.5mol/L |
| B、2mol/L |
| C、1.0mol/L |
| D、1.6mol/L |
不影响H2O的电离平衡的粒子是( )
A、 | ||
B、
| ||
C、 | ||
D、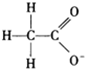 - - |
分子式为C4H8O2,且能发生水解反应的有机物有(不考虑立体异构)( )
| A、2种 | B、3种 | C、4种 | D、5种 |
下列各项比较中正确的是( )
| A、微粒半径:Na+>S2->O2- |
| B、结合质子的能力:ClO->CH3COO->HCO3- |
| C、固体的热稳定性:Na2CO3>CaCO3>NaHCO3 |
| D、碱性:NaOH>KOH>Mg(OH)2 |
在100g浓度为18mol/L、密度为ρ(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,如果水的密度为1g/cm3则加入水的体积( )
| A、小于100mL |
| B、等于100mL |
| C、大于100mL |
| D、不能确定 |
 一定质量的Na.K分别投入一定量的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a.b所示,则下列说法中正确的是( )
一定质量的Na.K分别投入一定量的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a.b所示,则下列说法中正确的是( )| A、投入的Na.K物质的质量一定相等 |
| B、曲线a对应的反应使用了催化剂 |
| C、曲线a代表K的反应,曲线b代表Na |
| D、两反应中盐酸必须是足量的 |