题目内容
6.在同温同压下,10mL气体A2和30mL气体B2完全反应可生成20mL气体C,则C的化学式为( )| A. | A2B6 | B. | A2B3 | C. | A3B | D. | AB3 |
分析 同温同压下,气体摩尔体积相等,同一方程式中,参加反应的各物质的体积之比等于其计量数之比,再结合原子守恒确定C的化学式.
解答 解:同温同压下,气体摩尔体积相等,同一方程式中,参加反应的各物质的体积之比等于其计量数之比,所以A2、B2、C计量数之比=10L:30L:20L=1:3:2,其方程式为A2+3B2=2C,根据原子守恒知,C的化学式为AB3,
故选D.
点评 本题考查质量守恒定律、阿伏伽德罗定律及其推论,侧重考查学生对基本理论的运用,明确计量数与体积的关系即可解答,题目难度不大.

练习册系列答案
相关题目
16. 八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
 八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )| A. | 莽草酸的分子之间可能发生酯化反应 | |
| B. | 莽草酸的分子式为C7H4O5 | |
| C. | 莽草酸中含有苯环 | |
| D. | 莽草酸不能使溴水褪色 |
17.不能实现下列物质间直接转换的是( )

| A. | 铝 | B. | 碳 | C. | 硫 | D. | 氮 |
14.下列说法正确的是( )
| A. | 用含有铁粉的透气小袋与食品一起密封包装,铁粉是常用的脱氧剂 | |
| B. | 浓硫酸可以盛放在铝桶中,说明铝不能与浓硫酸反应 | |
| C. | 过滤用到的玻璃仪器有铁架台、烧杯、漏斗、玻璃棒、滤纸 | |
| D. | 用氢氟酸雕刻玻璃,说明氢氟酸是强酸 |
1.在标准状况下,1体积水溶解224体积氨气,所得溶液密度为0.9g/cm3,这种氨水的物质的量浓度和质量分数分别为( )
| A. | 7.69mol/L 14.5% | B. | 8.15mol/L 15.4% | C. | 7.69mol/L 15.4% | D. | 8.17mol/L 14.5% |
11.在溶液中可以共存,加OH-产生沉淀,加H+生成气体的一组离子是( )
| A. | Na+、Cu2+、Cl-、CO32- | B. | HCO3-、Cl-、Fe3+、Na+ | ||
| C. | Cl-、K+、NO3-、Fe2+、 | D. | S2-、SO42-、NH4+、Fe2+ |
18.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1mol•L -1AgNO3,溶液:H+、K+、SO42-、I- | |
| B. | c( H+ )/c( OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| C. | 由水电离的 c(H+)=1×10-14mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| D. | 甲基橙呈红色的溶液中:Na+、CO32-、Fe3+、Cl- |
15.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1mol/LBaCl2溶液中含有的Ba2+数为NA | |
| B. | 1mol镁离子中含有的电子数为2NA | |
| C. | 常温常压下,11.2LH2中含有H2数为0.5NA | |
| D. | 16gO3中含有氧原子数为NA |
2.某有机化合物的结构简式为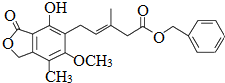 ,下列关于该化合物的说法不正确的是( )
,下列关于该化合物的说法不正确的是( )
 ,下列关于该化合物的说法不正确的是( )
,下列关于该化合物的说法不正确的是( )| A. | 该有机物的分子式为C23H24O6 | |
| B. | 1mol该化合物最多可以与9molH2发生加成反应 | |
| C. | 既可以使溴的四氯化碳溶液褪色,又可以使酸性KMnO4溶液褪色 | |
| D. | 既可以与FeCl3溶液发生显色反应,又可以与Na2CO3溶液反应 |