题目内容
11.在溶液中可以共存,加OH-产生沉淀,加H+生成气体的一组离子是( )| A. | Na+、Cu2+、Cl-、CO32- | B. | HCO3-、Cl-、Fe3+、Na+ | ||
| C. | Cl-、K+、NO3-、Fe2+、 | D. | S2-、SO42-、NH4+、Fe2+ |
分析 离子在溶液中可以大量共存,说明离子之间不发生任何反应,加OH-产生沉淀,溶液中可能存在Fe2+、Cu2+、Mg2+离子,加H+生成气体,说明溶液中可能存在CO32-或HCO3-离子或发生其它生成气体的反应,以此解答该题.
解答 解:A.Cu2+与CO32-反应生成沉淀而不能大量共存,故A错误;
B.HCO3-、Fe3+发生互促水解反应而不能大量共存,故B错误;
C.离子之间不发生任何反应,加OH-产生氢氧化亚铁沉淀,加H+发生氧化还原反应生成NO气体,符合题意,故C正确;
D.S2-、Fe2+反应生成沉淀而不能大量共存,故D错误.
故选C.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意与酸、碱的反应,题目难度不大.

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
6.在同温同压下,10mL气体A2和30mL气体B2完全反应可生成20mL气体C,则C的化学式为( )
| A. | A2B6 | B. | A2B3 | C. | A3B | D. | AB3 |
20.甲同学对Cl2与FeCl2和KSCN混合溶液的反应进行如下实验探究.请回答下列问题:
(1)装置B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(2)装置A中溶液变红的原因是2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3(用离子方程式表示).
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验:取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.甲同学的实验证明产生现象Ⅱ的原因是SCN-与Cl2发生了反应.甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为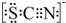
①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取装置A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素(填名称).
③通过实验证明了SCN-中氮元素转化为NO3-,则SCN-与Cl2反应生成1mol CO2,转移电子的物质的量是16mol.
④(SCN)2的性质与卤素单质相似,并且还原性按Br-<SCN-<I-的混合溶液中,反应的离子方程式为(SCN)2+2I-=I2+2SCN-.
| 操作 | 现象 |
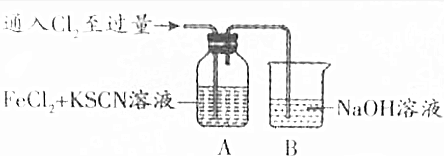 | Ⅰ.装置A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
(2)装置A中溶液变红的原因是2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3(用离子方程式表示).
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验:取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.甲同学的实验证明产生现象Ⅱ的原因是SCN-与Cl2发生了反应.甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
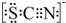
①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取装置A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素(填名称).
③通过实验证明了SCN-中氮元素转化为NO3-,则SCN-与Cl2反应生成1mol CO2,转移电子的物质的量是16mol.
④(SCN)2的性质与卤素单质相似,并且还原性按Br-<SCN-<I-的混合溶液中,反应的离子方程式为(SCN)2+2I-=I2+2SCN-.
 如图为氨气溶于水的喷泉实验装置(图中固定装置均已略去).
如图为氨气溶于水的喷泉实验装置(图中固定装置均已略去).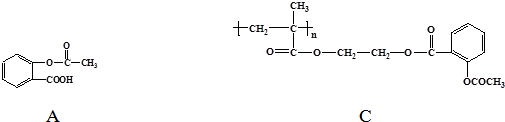
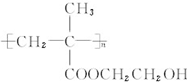 .
.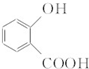 和CH3COOH(写结构简式).
和CH3COOH(写结构简式).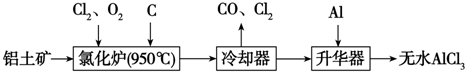


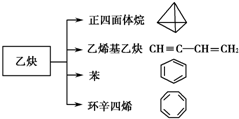 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物. .
. 、
、 .
.