题目内容
7.已知C(石墨)→C(金刚石)-Q,则可以判断( )| A. | 金刚石比石墨稳定 | B. | 石墨比金刚石稳定 | ||
| C. | 一样稳定 | D. | 无法判断 |
分析 根据C(石墨)→C(金刚石)-Q可知该反应为吸热反应,结合物质具有能量越低越稳定分析.
解答 解:已知C(石墨)→C(金刚石)-Q,说明该反应为吸热反应,则石墨具有的能量较低,所以石墨比金刚石稳定,
故选B.
点评 本题考查反应热与焓变的应用,题目难度不大,明确物质稳定性与具有能量的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
18.用NA表示阿伏加德罗常数的值.下列叙述错误的是( )
| A. | 常温下,1 L 0.1 mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 标准状况下,2.24 L 已烷中含有共价键的数目为1.9NA | |
| C. | 室温下,28.0 g乙烯和丁烯的混合气体中所含碳原子数为2NA | |
| D. | 足量Fe与1 mol Cl2充分反应,转移的电子数目为2NA |
15.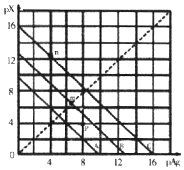 某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX、pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是( )
某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX、pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是( )
 某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX、pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是( )
某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX、pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是( )| A. | A线是AgCl的溶解平衡曲线 | |
| B. | 坐标点p形成的溶液是AgCl的不饱和溶液 | |
| C. | m点是在水中加入足量的AgBr形成的饱和溶液 | |
| D. | n点表示由过量的KI与AgNO3反应产生AgI沉淀 |
2.对于ⅣA族元素,下列叙述中不正确的是( )
| A. | CO2在常温下是气体,SiO2在常温下是固体 | |
| B. | C、Si、Ge的最外层电子数都是4,次外层电子数都是8 | |
| C. | CO2和SiO2都是酸性氧化物,在一定条件下都能和氧化钙反应 | |
| D. | 该族元素的主要化合价是+4和+2 |
12.将9.2g某芳香烃完全燃烧后的气体混合物通入过量的澄清石灰水中,石灰水共增重38g,然后过滤得到70g沉淀.已知该烃的相对原子质量小于100,下列说法不正确的是( )
| A. | 该烃的分子式为C7H8 | |
| B. | 该烃的含碳量大于乙烯的含碳量 | |
| C. | 该烃一氯代物有5种 | |
| D. | 该烃在光照或催化剂作用下能和氯气发生取代反应 |
19.五种短周期元素的某些性质如表所示,有关说法正确的是( )
| 元素 | 元素的相关信息 |
| M | 最高价氧化物对应水化物能与其气态氢化物反应生成盐 |
| W | 原子的M电子层上有3个电子 |
| X | 在短周期元素中,其原子半径最大 |
| Y | 最外层电子数是电子层数的2倍,且低价氧化物能与其气态氢化物反应生成Y的单质和H2O |
| Z | 元素最高正价与最低负价的代数和为6 |
| A. | M、Y、Z的简单离子半径依次增大 | |
| B. | W与Z形成的化合物属于离子化合物,其水溶液显酸性 | |
| C. | 化合物X2Y2、Y2Z2的晶体类型相同,化学键类型也相同 | |
| D. | M、W、X的最高价氧化物对应水化物两两之间能相互发生反应 |
16.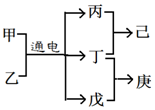 短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同周期,甲、乙、己是由这些元素组成的二元化合物,0.001mol•L-1的己溶液pH为3,庚是具有漂白性的混合物,上述物质的转化关系如图所示,下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同周期,甲、乙、己是由这些元素组成的二元化合物,0.001mol•L-1的己溶液pH为3,庚是具有漂白性的混合物,上述物质的转化关系如图所示,下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同周期,甲、乙、己是由这些元素组成的二元化合物,0.001mol•L-1的己溶液pH为3,庚是具有漂白性的混合物,上述物质的转化关系如图所示,下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同周期,甲、乙、己是由这些元素组成的二元化合物,0.001mol•L-1的己溶液pH为3,庚是具有漂白性的混合物,上述物质的转化关系如图所示,下列说法正确的是( )| A. | 原子半径Z>Y>X | |
| B. | 仅由这四种元素构成的溶液可能呈酸性、碱性或中性 | |
| C. | 己为由极性键构成的非极性分子 | |
| D. | 戊为一元弱碱 |
17. 在一定条件下,利用CO2合成CH3OH的反应如下:
在一定条件下,利用CO2合成CH3OH的反应如下:
CO2(g)+3H2(g)?H3OH(g)+H2O(g)△H1,
研究发现,反应过程中会有副反应:
CO2(g)+H2(g)?CO(g)+H2O(g)△H2.
温度对CH3OH、CO的产率影响如图所示.下列说法中,不正确的是( )
 在一定条件下,利用CO2合成CH3OH的反应如下:
在一定条件下,利用CO2合成CH3OH的反应如下:CO2(g)+3H2(g)?H3OH(g)+H2O(g)△H1,
研究发现,反应过程中会有副反应:
CO2(g)+H2(g)?CO(g)+H2O(g)△H2.
温度对CH3OH、CO的产率影响如图所示.下列说法中,不正确的是( )
| A. | △H1<0,△H2>0 | |
| B. | 增大压强有利于加快合成反应的速率 | |
| C. | 生产过程中,温度越高越有利于提高CH3OH的产率 | |
| D. | 合成CH3OH反应的平衡常数表达式是K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$ |
 (3)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图2:
(3)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图2: