题目内容
A、B、C、D是构成实验室中常见物质的4种元素,其中D元素是1826年一位法国科学家发现的,他在研究海水制盐时,向剩余的副产品苦卤中通入氯气后发现溶液颜色变深,进一步提取,得到一种红棕色有刺鼻臭味的液体;C元素原子比D元素原子少一个电子层,但是最外层电子数相同:A+和B2+都比C的离子少8个电子.回答下列问题:
(1)写出A、B、C、D的元素符号A ,B ,C ,D .
(2)画出A、C的原子结构示意图:
A ,C .
(3)你认为哪两种元素的原子最容易化合? ,写出这两种元素的单质反应的化学方程式 .
(4)用离子方程式表示从海水中提取D元素的单质的原理 .
(1)写出A、B、C、D的元素符号A
(2)画出A、C的原子结构示意图:
A
(3)你认为哪两种元素的原子最容易化合?
(4)用离子方程式表示从海水中提取D元素的单质的原理
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D四种元素,D元素的单质是一种红棕色液体,有刺鼻的臭味,则A单质是溴,则A元素是Br元素;
C元素原子比D元素原子少一个电子层,但是最外层电子数相同,说明C、D是同一主族元素,已知D为Br元素,则C为Cl元素;
A+和B2+都比C的离子少8个电子,C离子为氯离子,氯离子最外层含有18个电子,则A+和B2+核外的核外电子总数为10,故A为Na元素、B为Mg元素,据此进行解答.
C元素原子比D元素原子少一个电子层,但是最外层电子数相同,说明C、D是同一主族元素,已知D为Br元素,则C为Cl元素;
A+和B2+都比C的离子少8个电子,C离子为氯离子,氯离子最外层含有18个电子,则A+和B2+核外的核外电子总数为10,故A为Na元素、B为Mg元素,据此进行解答.
解答:
解:(1)A、B、C、D四种元素,D元素的单质是一种红棕色液体,有刺鼻的臭味,则A单质是溴,则A元素是Br元素;C元素原子比D元素原子少一个电子层,但是最外层电子数相同,说明C、D是同一主族元素,已知D为Br元素,则C为Cl元素;A+和B2+都比C的离子少8个电子,C离子为氯离子,氯离子最外层含有18个电子,则A+和B2+核外的核外电子总数为10,故A为Na元素、B为Mg元素,
根据分析可知,A为Na、B为Mg、C为Cl、D为Br元素,
故答案为:Na;Mg;Cl;Br;
(2)A为Na,其核电荷数为11,最外层含有1个电子,钠原子结构示意图为: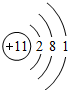 ;C为Cl元素,氯原子的核电荷数=核外电子总数=17,其原子结构示意图为:
;C为Cl元素,氯原子的核电荷数=核外电子总数=17,其原子结构示意图为: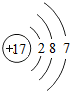 ,
,
故答案为: ;
; ;
;
(3)四种元素中,非金属性最强的Cl与金属性最强的Na元素最容易形成化合物NaCl,反应的化学方程式为:2Na+Cl2
2NaCl,
故答案为:Na和Cl;2Na+Cl2
2NaCl;
(4)氯气氧化性大于溴单质,氯气与溴离子反应生成溴单质和氯离子,从海水中提取溴元素的单质的原理为:Cl2+2Br-=2Cl-+Br2,
故答案为:Cl2+2Br-=2Cl-+Br2.
根据分析可知,A为Na、B为Mg、C为Cl、D为Br元素,
故答案为:Na;Mg;Cl;Br;
(2)A为Na,其核电荷数为11,最外层含有1个电子,钠原子结构示意图为:
 ;C为Cl元素,氯原子的核电荷数=核外电子总数=17,其原子结构示意图为:
;C为Cl元素,氯原子的核电荷数=核外电子总数=17,其原子结构示意图为: ,
,故答案为:
 ;
; ;
;(3)四种元素中,非金属性最强的Cl与金属性最强的Na元素最容易形成化合物NaCl,反应的化学方程式为:2Na+Cl2
| ||
故答案为:Na和Cl;2Na+Cl2
| ||
(4)氯气氧化性大于溴单质,氯气与溴离子反应生成溴单质和氯离子,从海水中提取溴元素的单质的原理为:Cl2+2Br-=2Cl-+Br2,
故答案为:Cl2+2Br-=2Cl-+Br2.
点评:本题考查了位置、结构与性质关系的综合应用,题目难度中等,正确推断各元素名称为解答关键,注意掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
常用的电池是一个液体电解质将两个固体电极隔开.而钠-硫(Na/S8)电池正相反,它是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+通过.下列有关说法不正确的是( )
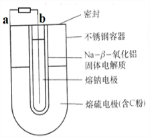

| A、a为电池的正极 |
| B、充电时b接电源的正极 |
| C、正极反应为:nS8+16ne-=8Sn2- |
| D、Na+可以穿过固体电解质和硫反应从而传递电流 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、1.0L1.0mol/L的Na2SO4水溶液中含有的氧原子数为4NA |
| B、1molNa2O2固体中含离子总数与1molCH4中所含共价键数目相等 |
| C、1molNaClO中所有ClO-的电子总数为26NA |
| D、标准状况下,6.72LNO2与水充分反应转移的电子数目为0.1NA |
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2和KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示.下列说法不正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2和KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示.下列说法不正确的是( )| A、反应I2(aq)+I-(aq)?I3-(aq)的△H<0 |
| B、状态A与状态B相比,状态A的c(I2)大 |
| C、若反应进行到状态D时,一定有V正>V逆 |
| D、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2 |
下列关于元素周期表的说法正确的是( )
| A、能生成碱的金属元素都在 IA族 |
| B、稀有气体元素原子的最外层电子数均为8 |
| C、第二周期 VIA族元素的原子核电荷数和中子数一定为8 |
| D、原子序数为14的元素位于元素周期表的第3周期ⅣA族 |
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196kJ?moL-1,一段时间后达平衡,反应过程中测定的部分数据见下表:下列说法不正确的是( )
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 2 | 1 |
| 5 | 1.2 | |
| 10 | 0.4 | |
| 15 | 0.8 |
| A、反应在前5min的平均速率为v (SO2)=0.08mol?L-1?min-1 |
| B、保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,v (正)>v (逆) |
| C、该温度,反应的平衡常数为11.25L?mol-1 |
| D、相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40% |
