题目内容
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196kJ?moL-1,一段时间后达平衡,反应过程中测定的部分数据见下表:下列说法不正确的是( )
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 2 | 1 |
| 5 | 1.2 | |
| 10 | 0.4 | |
| 15 | 0.8 |
| A、反应在前5min的平均速率为v (SO2)=0.08mol?L-1?min-1 |
| B、保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,v (正)>v (逆) |
| C、该温度,反应的平衡常数为11.25L?mol-1 |
| D、相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40% |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:A、根据化学反应速率v=
来计算;
B、温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,相当于增大压强,根据压强对化学平衡的影响来回答判断;
C、根据可逆反应不能进行彻底以及热化学方程式的意义来回答判断;
D、根据三行式计算化学反应中物质的转化率.
| △c |
| △t |
B、温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,相当于增大压强,根据压强对化学平衡的影响来回答判断;
C、根据可逆反应不能进行彻底以及热化学方程式的意义来回答判断;
D、根据三行式计算化学反应中物质的转化率.
解答:
解:A、根据已知数据,用二氧化硫化学反应速率v=
mol/(L?min)=0.08mol?L-1 min-1,故A正确;
B、温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,相当于增大压强,化学平衡正向移动,v(正)>v(逆),故B正确;
C、2SO2(g)+O2(g)?2SO3(g)
初始量(mol):2 1 0
变化量(mol):1.2 0.6 1.2
平衡量(mol):0.8 0.4 1.2
容器体积为2L,化学平衡常数K=
=
=5.65,故C错误;
D、起始时向容器中充入1.5mol SO3,如果转化率是40%,则
2SO2(g)+O2(g)?2SO3(g)
初始量(mol/L):0 0 0.75
变化量(mol/L):0.3 0.15 0.3
平衡量(mol/L):0.3 0.15 0.45
则
=
,故D正确;
故选C.
| ||
| 5 |
B、温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,相当于增大压强,化学平衡正向移动,v(正)>v(逆),故B正确;
C、2SO2(g)+O2(g)?2SO3(g)
初始量(mol):2 1 0
变化量(mol):1.2 0.6 1.2
平衡量(mol):0.8 0.4 1.2
容器体积为2L,化学平衡常数K=
| 0.62 |
| 0.42×0.2 |
| 45 |
| 8 |
D、起始时向容器中充入1.5mol SO3,如果转化率是40%,则
2SO2(g)+O2(g)?2SO3(g)
初始量(mol/L):0 0 0.75
变化量(mol/L):0.3 0.15 0.3
平衡量(mol/L):0.3 0.15 0.45
则
| 0.452 |
| 0.32×0.15 |
| 45 |
| 8 |
故选C.
点评:本题涉及等效平衡的建立以及化学反应达到平衡时物质的转化率等方面的知识,属于综合知识的考查,难度大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关化学用语使用正确的是( )
A、硫离子的原子结构示意图  | ||
| B、氯离子的电子式:Cl- | ||
C、原子核内有10个中子的氧原子:
| ||
| D、二氧化硫溶于水的反应化学方程式:SO2+H2O═H2SO4 |
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)?N2O5(g)+O2(g)有关说法正确的是( )
| A、升高温度可减小反应速率 |
| B、加入合适的催化剂可提高反应速率 |
| C、达到平衡时,v(正)=v(逆)=0 |
| D、达到平衡时,NO2转化率为100% |
下列变化属于物理变化的是( )
| A、用石油分馏炼制汽油 |
| B、用煤干馏制备焦炭 |
| C、用铝土矿冶炼铝 |
| D、用海带提取碘单质 |
下列食用品的有效成分正确的是( )
A、 C6H12O6 |
B、 Na2CO3 |
C、 CH3COOH |
D、 Al(OH)3 |
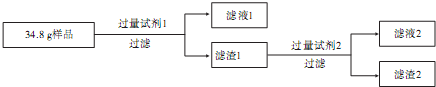
 二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水.实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水.实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
