题目内容
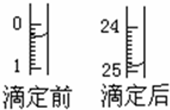 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定法测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定法测定其浓度.(1)滴定
①用
②有关数据记录如表:
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | 25.00 | 0.50 | 24.95 | 24.45 |
| 2 | 25.00 | |||
| 3 | 25.00 | 6.00 | 30.55 | 24.55 |
(3)下列操作会造成测定结果(待测NaOH溶液浓度值)偏低的有
A.酸式滴定管水洗后未用标准稀盐酸溶液润洗
B.锥形瓶水洗后直接装待测液
C.摇动锥形瓶时有少量液体溅出瓶外
D.滴定到达终点时,俯视读出滴定管读数;
E.酸式滴定管尖嘴部分有气泡,滴定后消失.
考点:中和滴定
专题:实验题
分析:(1)①根据酸性溶液存放在酸式滴定管中;②根据滴定管的结构以及测量体积的原理来分析.
(2)先考虑数据的合理性,然后求体积的平均值,然后根据c(待测)=
计算;
(3)根据c(待测)=
分析误差.
(2)先考虑数据的合理性,然后求体积的平均值,然后根据c(待测)=
| C(标准)C(标准) |
| C(待测) |
(3)根据c(待测)=
| C(标准)C(标准) |
| C(待测) |
解答:
解:(1)①盐酸是酸性溶液,存放在酸式滴定管中,故答案为:酸;
②滴定前读数为0.30mL,滴定后读数为24.90mL,消耗溶液的体积为24.60mL,故答案为:0.30mL,24.90mL,24.60mL;
(2)求出第1组、第2组、第3组消耗的盐酸标准液的体积为:
mL=24.53mL,c(待测)=
=
mol/L=0.098mol/L,故答案为:0.098mol/L;
(3)A.酸式滴定管水洗后未用标准稀盐酸溶液润洗,导致标准液的浓度减小,消耗的标准液体积偏大,测定结果偏高,故A错误;
B.锥形瓶水洗后直接装待测液,消耗的标准液体积无影响,测定结果无影响,故B错误;
C.摇动锥形瓶时有少量液体溅出瓶外,消耗的标准液体积偏小,测定结果偏小,故C正确;
D.滴定到达终点时,俯视读出滴定管读数,消耗的标准液体积偏小,测定结果偏小,故D正确;
E.酸式滴定管尖嘴部分有气泡,滴定后消失,消耗的标准液体积偏大,测定结果偏高,故E错误;
故选:CD.
②滴定前读数为0.30mL,滴定后读数为24.90mL,消耗溶液的体积为24.60mL,故答案为:0.30mL,24.90mL,24.60mL;
(2)求出第1组、第2组、第3组消耗的盐酸标准液的体积为:
| 24.45+24.60+24.55 |
| 3 |
| C(标准)C(标准) |
| C(待测) |
| 24.53×0.1000 |
| 25.00 |
(3)A.酸式滴定管水洗后未用标准稀盐酸溶液润洗,导致标准液的浓度减小,消耗的标准液体积偏大,测定结果偏高,故A错误;
B.锥形瓶水洗后直接装待测液,消耗的标准液体积无影响,测定结果无影响,故B错误;
C.摇动锥形瓶时有少量液体溅出瓶外,消耗的标准液体积偏小,测定结果偏小,故C正确;
D.滴定到达终点时,俯视读出滴定管读数,消耗的标准液体积偏小,测定结果偏小,故D正确;
E.酸式滴定管尖嘴部分有气泡,滴定后消失,消耗的标准液体积偏大,测定结果偏高,故E错误;
故选:CD.
点评:本题主要考查了中和滴定操作、化学计算以及注意事项,难度不大,分析误差时要看是否影响标准体积的用量,若标准体积偏大,结果偏高;若标准体积偏小,则结果偏小;若不影响标准体积,则结果无影响.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知热化学方程式:Zn(s)+
O2═ZnO(s)△H=-akJ?mol-1 2Hg(l)+O2(g)═2HgO(s)△H=-bkJ.mol-1由此可知Zn(s)+HgO(s)═ZnO(s)+Hg(l)△H=( )
| 1 |
| 2 |
A、
| ||
B、
| ||
| C、2a-bkJ?mol-1 | ||
| D、b-2akJ?mol |
下列操作方法或实验装置正确的是( )
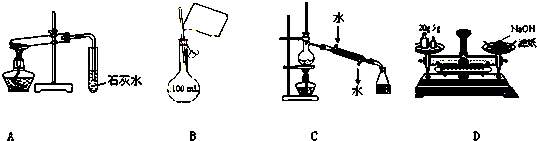

| A、装置探究NaHCO3的热稳定性 |
| B、配制100 mL 0.10 mol?L-1NaCl溶液 |
| C、实验室用该装置制取少量蒸馏水 |
| D、称量25 g NaOH |
在4份碘化钾淀粉溶液中,分别加入下列物质,不能使溶液变蓝的是( )
| A、氯化氢 | B、溴水 |
| C、氯气 | D、碘的酒精溶液 |

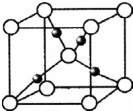 A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素.已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个单电子,G的核电荷数比F多5.请回答下列问题(用相应的元素符号、化学式和化学术语填空)
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素.已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个单电子,G的核电荷数比F多5.请回答下列问题(用相应的元素符号、化学式和化学术语填空) 实验室有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:
实验室有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验: