题目内容
13.下列化学用语正确的是( )| A. | 电离方程式:Na2SO4═Na2++SO42- | B. | 氯化钠的电子式: | ||
| C. | 14C的原子结构示意图: | D. | CH4分子的比例模型: |
分析 A.电离方程式中,两个钠离子不能合并;
B.氯离子为阴离子,电子式中需要标出最外层电子;
C.该碳原子的核电荷数为6,最外层含有4个电子;
D.比例模型只要体现出各原子的相对体积大小,甲烷分子中碳原子的相对体积大于氢原子.
解答 解:A.硫酸钠在溶液中电离出钠离子和硫酸根离子,其电离方程式为:Na2SO4=2Na++SO42-,故A错误;
B.氯化钠为离子化合物,钠离子直接用离子符号表示,氯离子需要标出最外层电子及所带电荷,氯化钠正确的电子式为 ,故B错误;
,故B错误;
C.14C的核电荷数为6,最外层电子数为4,其正确的原子结构示意图为: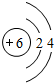 ,故C错误;
,故C错误;
D.甲烷为正四面体结构,C原子的相对体积大于H原子,其比例模型为: ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的判断,题目难度中等,涉及电子式、原子结构示意图、比例模型、电离方程式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.在恒容密闭容器中进行合成氨反应:N2(g)+3H2(g)═2NH3(g)△H<0,其平衡常数K与温度T的关系如下:
(1)K1>K2(填“>”、“<”或“=”)
(2)下列各项可说明反应达到平衡状态的是ce
a.容器内N2、H2、NH3浓度比为1:3:2 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体密度保持不变
e.混合气体平均摩尔质量保持不变
(3)某温度下,在1L恒温恒容容器中充入1mol N2和3mol H2进行上述反应,10min达平衡,此时容器内压强变为原来的$\frac{7}{8}$.
①该过程的平均反应速率v(NH3)=0.05mol•L-1•min-1
②N2的平衡转化率为25%.
| T/K | 298 | 398 | 498 |
| 平衡常数K/L2•mol-2 | 4.1×106 | K1 | K2 |
(2)下列各项可说明反应达到平衡状态的是ce
a.容器内N2、H2、NH3浓度比为1:3:2 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体密度保持不变
e.混合气体平均摩尔质量保持不变
(3)某温度下,在1L恒温恒容容器中充入1mol N2和3mol H2进行上述反应,10min达平衡,此时容器内压强变为原来的$\frac{7}{8}$.
①该过程的平均反应速率v(NH3)=0.05mol•L-1•min-1
②N2的平衡转化率为25%.
4.下列物质中属于电解质的是( )
| A. | C12H22O11(蔗糖) | B. | CO2 | C. | NaCl | D. | Al |
1.下列设计的实验方案能达到实验目的是( )
| A. | 制备干燥的NH3:加热浓氨水,将生成的气体通过盛有浓硫酸的洗气瓶 | |
| B. | 提纯含有少量HCl的CO2:将混合气体依次通过盛有饱和碳酸钠溶液、浓硫酸的洗气瓶 | |
| C. | 检验食盐中是否含有碘酸钾:取少量的食盐溶液,加稀硫酸酸化,再滴入淀粉溶液,观察实验现象 | |
| D. | 探究温度对化学平衡移动的影响:将盛有NO2和N2O4混合气体的烧瓶,先后置于冷水和热水中,观察烧瓶中气体颜色的变化 |
18.通过一步反应不能实现下列转化的是( )
| A. | Na2CO3→NaHCO3 | B. | Fe→FeCl2 | C. | NaCl→Na | D. | Al2O3→Al(OH)3 |
5.一定浓度200mL的HNO3溶液中加入5.6g Fe,全部溶解,得到标准状况下的NO气体2.24L,测得反应后溶液中的c(H+)=0.1mol/L.若反应前后溶液体积变化忽略不计,则下列有关判断正确的是( )
| A. | 反应前HNO3溶液的浓度为2.0mol•L-1 | |
| B. | 反应后溶液中含硝酸亚铁 | |
| C. | 反应后的溶液最多还能溶解3.22g Fe | |
| D. | 反应后溶液中c(NO3-)=1.5mol•L-1 |
3.某酸式盐NaHY的水溶液中存在c(OH-)>c(H+),则下列叙述正确的是( )
| A. | H2Y的电离方程式:H2Y?2H++Y2- | |
| B. | HY-的水解方程式:HY-+H2O?H3O++Y2- | |
| C. | 该酸式盐溶液中粒子浓度关系:c(Na+)>c(HY-)>c(OH-)>c(H2Y)>c(H+) | |
| D. | 该酸式盐溶液中离子浓度关系:c(Na+)>c(Y2-)>c(HY-) |
 电解饱和食盐水所得溶液经多次循环使用后,ClO-、ClO${\;}_{3}^{-}$含量会增加.
电解饱和食盐水所得溶液经多次循环使用后,ClO-、ClO${\;}_{3}^{-}$含量会增加.