题目内容
18.通过一步反应不能实现下列转化的是( )| A. | Na2CO3→NaHCO3 | B. | Fe→FeCl2 | C. | NaCl→Na | D. | Al2O3→Al(OH)3 |
分析 A、碳酸钠与二氧化碳水溶液反应生成碳酸氢钠;
B、铁与三氯化铁反应生成氯化亚铁;
C、电解熔融氯化钠可以生成钠;
D、Al2O3到Al(OH)3不能一步反应实现.
解答 解:A、碳酸钠与二氧化碳水溶液反应生成碳酸氢钠,可以一步实现,符合题意要求,故不选;
B、铁与三氯化铁反应生成氯化亚铁,可以一步实现,符合题意要求,故不选;
C、电解熔融氯化钠可以生成钠,能一步反应实现,符合题意,故不选;
D、氧化铝属两性氧化物,能与酸或者碱发生复分解反应生成盐和水.上述反应中没有Al(OH)3这种碱的生成,因此由Al2O3到Al(OH)3不能一步反应实现,故选;
故选D.
点评 熟练掌握常见物质的性质与变化规律,是解答此类问题的基本的知识基础.

练习册系列答案
相关题目
13.下列化学用语正确的是( )
| A. | 电离方程式:Na2SO4═Na2++SO42- | B. | 氯化钠的电子式: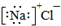 | ||
| C. | 14C的原子结构示意图: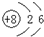 | D. | CH4分子的比例模型: |
3.下列对各物质性质的解释不正确的是
( )
| 选项 | 性质 | 原因 |
| A | Fe与稀HNO3、稀H2SO4反应均有气泡产生 | Fe与两种酸均发生置换反应 |
| B | 加热铝箔,熔化的铝不滴落 | 铝表面的氧化膜熔点高,包在熔化的铝外面 |
| C | 重金属盐中毒可服用牛奶解毒 | 牛奶中蛋白质变性,保护了人体的蛋白质 |
| D | 明矾用来净水 | Al3+水解生成Al(OH)3胶体,具有吸附性 |
| A. | A | B. | B | C. | C | D. | D |
7.在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体[(NH4)2SO4•FeSO4•6H2O](式量为392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇.
(1)为洗涤(NH4)2SO4•FeSO4•6H2O粗产品,下列方法中最合适的是D.
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
(2)为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定.每次所取待测液体积均为25.00mL,实验结果记录如下:
滴定过程中发生反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O.滴定终点的现象是滴入最后一滴高锰酸钾溶液,锥形瓶内溶液由浅绿色变为浅紫色,且30s不变色.通过实验数据计算的该产品纯度为$\frac{980c}{a}$×100%(用字母ac表).上表中第一次实验中记录数据明显大于后两次,其原因可能是BC(填符号).
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低.
(1)为洗涤(NH4)2SO4•FeSO4•6H2O粗产品,下列方法中最合适的是D.
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
(2)为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定.每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低.
8.下列离子方程式书写正确的是( )
| A. | 醋酸滴在石灰石上:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铁与稀盐酸反应 2Fe+6H+=2Fe3++3H2↑ | |
| C. | 铜片插入硝酸银溶液中:Cu+2Ag+═2Ag+Cu2+ | |
| D. | 硫酸铜与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
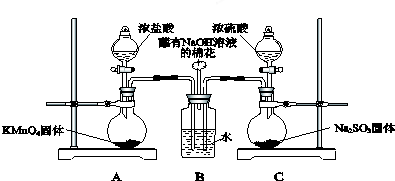
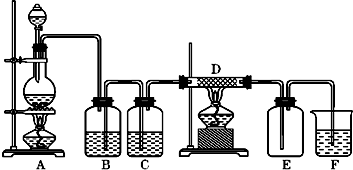
 .
.