题目内容
15.实验室中可用如下反应制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应中氧化剂与还原剂的物质的量之比为( )| A. | 1:8 | B. | 5:2 | C. | 1:5 | D. | 5:1 |
分析 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,通过化合价升降判断,Mn元素由+7价降低到+2价,Cl元素的化合价由-1价升高到0,高锰酸钾得电子是氧化剂,利用电子的转移与结合方程式进行计算.
解答 解:反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素由+7价降低到+2价,Cl元素的化合价由-1价升高到0,2mol高锰酸钾在反应中得电子,为氧化剂,10molHCl(另外的6molHCl表现酸性)失电子是还原剂,所以氧化剂与还原剂的物质的量之比是2:10=1:5,
故选C.
点评 本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,为高频考点,题目难度中等,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质.

练习册系列答案
相关题目
3.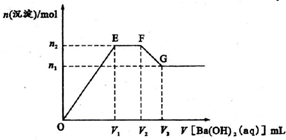 在A12(SO4)3和NH4Cl等物质的量浓度的混合溶液中,逐滴加人Ba(OH)2溶液,淀的物质的量与Ba(OH)2溶液的体积的关系如图所示.下列说法不正确的是( )
在A12(SO4)3和NH4Cl等物质的量浓度的混合溶液中,逐滴加人Ba(OH)2溶液,淀的物质的量与Ba(OH)2溶液的体积的关系如图所示.下列说法不正确的是( )
 在A12(SO4)3和NH4Cl等物质的量浓度的混合溶液中,逐滴加人Ba(OH)2溶液,淀的物质的量与Ba(OH)2溶液的体积的关系如图所示.下列说法不正确的是( )
在A12(SO4)3和NH4Cl等物质的量浓度的混合溶液中,逐滴加人Ba(OH)2溶液,淀的物质的量与Ba(OH)2溶液的体积的关系如图所示.下列说法不正确的是( )| A. | EF段反应的离子方程式为:NH4++OH-=NH3•H2O | |
| B. | G点沉淀为BaSO4 | |
| C. | F点反应体系的溶液中溶质的种类比E点多 | |
| D. | n2:nl=3:2 |
10.下列气体遇空气变红棕色的是( )
| A. | SO2 | B. | Cl2 | C. | CO2 | D. | NO |
20.下列说法不正确的是( )
| A. | Na2CO3比NaHCO3溶解度大 | |
| B. | Na2CO3比NaHCO3稳定 | |
| C. | Na2CO3和NaHCO3都能跟石灰水反应得到白色沉淀 | |
| D. | 物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应得CO2物质的量之比为2:1 |
7.欲用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,下列有关说法正确的是( )
| A. | 滴定管在装溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 | |
| B. | 锥形瓶在装待测溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 | |
| C. | 滴定过程中,两眼注视滴定管装液面的变化 | |
| D. | 装标准液的滴定管中有气泡而滴定前未排出,则滴定结果将偏低 |
4.能源是国民经济发展的重要物质基础,下列有关能源的说法错误的是( )
| A. | 我国目前使用的主要能源是煤、石油和天然气 | |
| B. | 解决能源危机的方法是开发新能源和节约现有能源,提高能源的利用率 | |
| C. | 开发的新能源包括太阳能、氢能、核能等,它们都是可再生能源 | |
| D. | 提高燃料利用率的方式是科学控制反应,使燃料充分燃烧 |
5.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 0.1 mol溴苯中含有双键的数目为0.3NA | |
| B. | 标准状况下,22.4 L己烷中含己烷分子数目为NA | |
| C. | 1mol甲醇中含有C-H键的数目为4NA | |
| D. | 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA |