题目内容
3.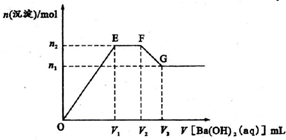 在A12(SO4)3和NH4Cl等物质的量浓度的混合溶液中,逐滴加人Ba(OH)2溶液,淀的物质的量与Ba(OH)2溶液的体积的关系如图所示.下列说法不正确的是( )
在A12(SO4)3和NH4Cl等物质的量浓度的混合溶液中,逐滴加人Ba(OH)2溶液,淀的物质的量与Ba(OH)2溶液的体积的关系如图所示.下列说法不正确的是( )| A. | EF段反应的离子方程式为:NH4++OH-=NH3•H2O | |
| B. | G点沉淀为BaSO4 | |
| C. | F点反应体系的溶液中溶质的种类比E点多 | |
| D. | n2:nl=3:2 |
分析 在A12(SO4)3和NH4Cl等物质的量浓度的混合溶液中逐滴加人Ba(OH)2溶液,首先发生反应2Ba2++6OH-+2Al3++2SO42-═2BaSO4↓+Al(OH)3↓(OE段);当钡离子、铝离子完全沉淀时,发生反应NH4++OH-=NH3•H2O(EF段),此段沉淀的量不变;FG段:当铵根离子反应完全后,发生反应OH-+Al(OH)3=AlO2-+2H2O,之至氢氧化铝沉淀完全溶解,最终剩余的沉淀为硫酸钡据此进行解答.
解答 解:在A12(SO4)3和NH4Cl等物质的量浓度的混合溶液中逐滴加人Ba(OH)2溶液,OB段:首先发生反应:2Ba2++6OH-+2Al3++2SO42-═2BaSO4↓+Al(OH)3↓;
EF段:当钡离子、铝离子完全沉淀时,发生反应:NH4++OH-=NH3•H2O,此段沉淀的量不变;
FG段:当铵根离子反应完全后,发生反应:OH-+Al(OH)3=AlO2-+2H2O,氢氧化铝沉淀之至完全溶解,最终剩余的沉淀为硫酸钡,
A.根据分析可知,EF段反应的离子方程式为:NH4++OH-=NH3•H2O,故A正确;
B.G点氢氧化铝沉淀完全溶解,此时剩余的沉淀为BaSO4,故B正确;
C.E点沉淀恰好达到最大,溶质为氯化铵,F点铵根离子恰好完全反应,溶质为一水合氨和氯化钡,所以F点反应体系的溶液中溶质的种类比E点多,故C正确;
D.n2为氢氧化铝和硫酸钡沉淀,nl为硫酸钡沉淀,根据化学式A12(SO4)3可知n2:nl=5:3,故D错误;
故选D.
点评 本题考查了混合物反应的计算,题目难度中等,明确图象曲线变化的含义为解答关键,注意掌握离子反应发生的先后顺序,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
19.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、NO3-、Cl-、Na+ | |
| B. | 水电离出的c(H+)=10-12mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的水溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | 中性溶液中:Na+、Cl-、Fe3+、SO42- |
14.下列物质的变化,不能通过一步化学反应完成的是( )
| A. | N2→NH3 | B. | SiO2→Na2SiO3 | C. | Na2O2→Na2CO3 | D. | SiO2→H2SiO3 |
11.下列关于钠的说法中不正确的是( )
| A. | 金属钠和氧气反应,条件不同,产物则不同 | |
| B. | 将钠投入氯化铵溶液中会有无色有刺激性气味的气体生成 | |
| C. | 当钠与硫酸铜溶液反应时,有大量红色固体铜生成 | |
| D. | 钠的化学性质比较活泼,少量的钠可以保存煤油中 |
18.下列有关说法错误的是( )
| A. | 清晨在树林中有可能观察到丁达尔效应 | |
| B. | 一般情况下溶液中的溶质不会自动与溶剂分离 | |
| C. | 分散质粒子直径在1×10-7~1×10-5cm的分散系叫做胶体 | |
| D. | 饱和抓化铁溶液加热煮沸可制得Fe(OH)3胶体 |
8.下列关于粒子结构的描述不正确的是( )
| A. | H2S和NH3均是价电子总数为8的极性分子 | |
| B. | OH-和HF均是含有极性键的10电子粒子 | |
| C. | CHCl3和CCl4均是四面体构型的非极性分子 | |
| D. | 1 mol D216O(重水)中含中子、质子、电子各10NA(NA代表阿伏加德罗常数的值) |
15.实验室中可用如下反应制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应中氧化剂与还原剂的物质的量之比为( )
| A. | 1:8 | B. | 5:2 | C. | 1:5 | D. | 5:1 |
12.光纤通信是以光作为信息的载体,让光在光导纤维中传播,制造光导纤维的原料是( )
| A. | 银 | B. | 铜 | C. | 铝 | D. | 石英砂 |
13.下列化学实验中的操作、现象及结论都正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向甲苯中滴入少量浓溴水,充 分振荡,静置 | 下层接近无色 | 说明甲苯与溴发生了 取代反应 |
| B | 向蛋白质溶液中加入适量 CuSO4溶液并充分混合 | 溶液中有沉淀析出 | 可用CuSO4溶液分离、提纯蛋白质 |
| C | 溴乙烷与NaOH水溶液混合共热后,再加入稀硝酸至溶液呈酸性,滴入硝酸银溶液 | 溶液中出现淡黄色沉淀 | 说明溴乙烷中含有溴元素 |
| D | 向适量淀粉溶液中加入少量稀硫酸,加热约5 min,冷却后再加入新制Cu(OH)2浊液并加热 | 混合液中无红色沉淀出现 | 说明淀粉没有发生水解反应生成葡萄糖 |
| A. | A | B. | B | C. | C | D. | D |