题目内容
2.不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示.下列有关说法不正确的是( )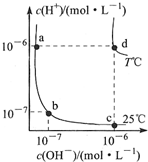
| A. | d点对应的食盐水pH=6,呈中性 | |
| B. | 向a点对应的醋酸溶液中滴加NaOH溶液至b点,此时c(Na+)=c(CH3COO-) | |
| C. | T℃时,0.05mol/LBa(OH)2溶液的pH=11 | |
| D. | a点对应的稀硫酸与c点对应的CH3COONa溶液中水的电离程度相同 |
分析 A、d点所在的温度下,水的离子积Kw=10-12;
B、向a点对应的醋酸溶液中滴加NaOH溶液至b点,溶液显中性,即c(H+)=c(OH-);
C、T℃时,水的离子积Kw=10-12.
D、酸对水的电离有抑制作用,盐的水解对水的电离有促进作用.
解答 解:A、d点所在的温度下,水的离子积Kw=10-12,而食盐水溶液永远显中性,故在d点温度下,食盐水的pH=6,故A正确;
B、向a点对应的醋酸溶液中滴加NaOH溶液至b点,溶液显中性,即c(H+)=c(OH-),而根据电荷守恒可知:
c(H+)+c(Na+)=c(CH3COO-)+c(OH-),故有c(Na+)=c(CH3COO-),故B正确;
C、T℃时,水的离子积Kw=10-12,0.05mol/LBa(OH)2溶液中,氢氧根的浓度c(OH-)=0.1mol/L,则有:c(H+)=10-11mol/L,则pH=11,故C正确;
D、酸对水的电离有抑制作用,盐的水解对水的电离有促进作用,故a点对应的稀硫酸溶液中水的电离程度小于醋酸钠溶液中的水的电离程度,故D错误.
故选D.
点评 本题考查了水的离子积和盐类水解中的电荷守恒以及酸碱和盐的水解对水的电离的影响,难度中等,属于高考常考的题型.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
12.《天工开物》中有关炼铁方法的记载是“凡炉中炽铁用炭,煤炭居十七,木炭居十三.凡山林无煤之处,锻工先选择坚硬条木,烧成火墨,其炎更烈于煤.即用煤炭.也别有铁炭一种.取其火性内攻,焰不虚腾者,与炊炭同形而分类也.”.下列有关说法错误的是( )
| A. | 用炭炽铁,炭是还原剂 | B. | 炽铁用炭,煤炭占17% | ||
| C. | 火墨燃烧温度比煤高 | D. | 炽铁不能用炊炭 |
17.下列物质一定属于同系物的是( )
①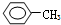
②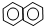
③
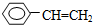
④C2H4
⑤CH2=CH-CH=CH2
⑥C3H6
⑦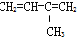
⑧
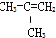
①

②
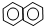
③
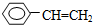
④C2H4
⑤CH2=CH-CH=CH2
⑥C3H6
⑦
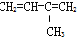
⑧
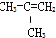
| A. | ④和⑥ | B. | ①、②和③ | C. | ⑤和⑦ | D. | ⑥和⑧ |
7.下列晶体熔化时不需要破坏化学键的是( )
| A. | 金刚石 | B. | 氟化镁 | C. | 冰 | D. | 金属钾 |
14.已知A、B、C、D、E是短周期中原子序数一次增大5种主族元素,其中元素A、E的单 质常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料,下列说法正确的是( )
| A. | 原子半径:A<B<C<D<E | |
| B. | 化合物AE与CE含有相同类型的化学键 | |
| C. | 金属性:D>C | |
| D. | D单质能够溶解于C的最高价氧化物对应的水化物 |
11.已知 X、Y、Z、M、R五种元素中,原子序数X<Y<Z<M<R,其结构或性质信息如下表.请根据信息回答有关问题:
(1)元素M的原子核外共有17种不同运动状态的电子,有5种不同能级的电子.
(2)X、Y、Z三种元素的第一电离能较高的是N(写元素符号),原因是N原子的2p能级电子为半充满,为较稳定的结构.
(3)R的一种配合物的化学式为RCl3•6H2O.已知0.01molRCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是B.
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2•H2O C.[R(H2O)4Cl2]Cl•2H2O D.[R(H2O)3Cl3]•3H2O.
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数. |
| Y | 原子核外的L层有3个未成对电子. |
| Z | 在元素周期表的各元素中电负性仅小于氟. |
| M | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子. |
| R | 第四周期过渡元素,其价电子层各能级处于半充满状态 |
(2)X、Y、Z三种元素的第一电离能较高的是N(写元素符号),原因是N原子的2p能级电子为半充满,为较稳定的结构.
(3)R的一种配合物的化学式为RCl3•6H2O.已知0.01molRCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是B.
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2•H2O C.[R(H2O)4Cl2]Cl•2H2O D.[R(H2O)3Cl3]•3H2O.
12.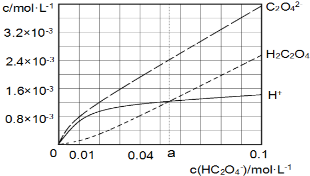 25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )
25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )
 25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )
25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )| A. | 当c(HC2O4ˉ)=0.1mol•Lˉ1时,c(H+)>c(C2O42-)-c(H2C2O4) | |
| B. | 当c(HC2O4ˉ)>amol•Lˉ1时,c(H+)<c(H2C2O4),HC2O4ˉ的水解程度大于电离程度 | |
| C. | HC2O4ˉ?C2O42-+H+,Ka(HC2O4ˉ)=a | |
| D. | 将0.08mol•Lˉ1H2C2O4溶液与等浓度NaOH溶液等体积混合后(忽略体积变化),c(Na+)>c(HC2O4ˉ)>c(C2O42-)>c(H2C2O4)>c(H+)>c(OHˉ) |