题目内容
1.下列反应的离子方程式书写正确的是( )| A. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| B. | 稀硫酸与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 盐酸与氢氧化钠溶液反应:H++OH-═H2O | |
| D. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ |
分析 A.漏掉了氢离子与氢氧根离子生成水的反应;
B.铁与稀硫酸反应生成硫酸亚铁,不是生成铁离子;
C.氢氧化钠与盐酸反应生成氯化钠和水;
D.碳酸钙为难溶物,离子方程式中不能拆开.
解答 解:A.氢氧化钡与硫酸反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故A错误;
B.稀硫酸与铁粉反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.盐酸与氢氧化钠溶液反应的离子方程式为:H++OH-═H2O,故C正确;
D.碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故D错误;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.图为工业合成氨生产简易流程图:
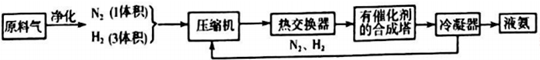
回答下列问题:
(1)合成氨所需的氮气来源于空气;合成氨所需的原料气氢气可由天然气制备,其主要反应为CH4(g)+H2O(g)=CO(g)+3H2(g);CH4和O2的反应:2CH4(g)+O2(g)=2CO(g)+4H2(g).CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气中氧气含量不同)混合反应,产物气体组成如表:
计算该富氧空气中O2和N2的体积比V(O2):V(N2)=2:3.
(2)在合成氨的原科气中混有的杂质必须除去的原因是防止催化剂中毒;
上述流程中热交换器的作用是热交换器是利用合成氨和氨冷凝放出的热量来加热原料气体或预热反应混合气.从合成塔出来的混合气体,通常仅含有15%(体积分数)的氨.为提高原料的利用率,通常采取的措施是将N2,H2循环利用.
(3)合成氮为放热反应,但工业上采用400℃-500℃的温度,主要原因是:
①该温度范围内反应速率较快.②该温度下催化剂的活性较大.
(4)氨可与CO2反应制备尿素(CO(NH2)2],反应过程分为两步,试写出有关的化学方程式:
①氮气与二氧化碳在加热加压条件下化合生成氨基甲酸铵(H2NCOONH4):2NH3+CO2$\stackrel{加热加压}{→}$H2NCOONH4.
②氨基甲酸铵受热分解为尿素与水:H2NCOONH4$\stackrel{△}{→}$CO(NH2)2+H2O.
(5)新法合成氨常采用电解法合成.即常压下将氢气和用氢气稀释的氮气分别通入一个加热到570℃的电解池中,氢气和氮气在电极上合成了氨,大大提高了氨的产率.新法合成氨所用的电解质能传导H+,则阴极的电极反应式为N2+6H++6e-═2NH3.

回答下列问题:
(1)合成氨所需的氮气来源于空气;合成氨所需的原料气氢气可由天然气制备,其主要反应为CH4(g)+H2O(g)=CO(g)+3H2(g);CH4和O2的反应:2CH4(g)+O2(g)=2CO(g)+4H2(g).CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气中氧气含量不同)混合反应,产物气体组成如表:
| 气体 | CO | H2 | N2 | O2 |
| 体积(L) | 25 | 60 | 15 | 2.5 |
(2)在合成氨的原科气中混有的杂质必须除去的原因是防止催化剂中毒;
上述流程中热交换器的作用是热交换器是利用合成氨和氨冷凝放出的热量来加热原料气体或预热反应混合气.从合成塔出来的混合气体,通常仅含有15%(体积分数)的氨.为提高原料的利用率,通常采取的措施是将N2,H2循环利用.
(3)合成氮为放热反应,但工业上采用400℃-500℃的温度,主要原因是:
①该温度范围内反应速率较快.②该温度下催化剂的活性较大.
(4)氨可与CO2反应制备尿素(CO(NH2)2],反应过程分为两步,试写出有关的化学方程式:
①氮气与二氧化碳在加热加压条件下化合生成氨基甲酸铵(H2NCOONH4):2NH3+CO2$\stackrel{加热加压}{→}$H2NCOONH4.
②氨基甲酸铵受热分解为尿素与水:H2NCOONH4$\stackrel{△}{→}$CO(NH2)2+H2O.
(5)新法合成氨常采用电解法合成.即常压下将氢气和用氢气稀释的氮气分别通入一个加热到570℃的电解池中,氢气和氮气在电极上合成了氨,大大提高了氨的产率.新法合成氨所用的电解质能传导H+,则阴极的电极反应式为N2+6H++6e-═2NH3.
16.下列物质的性质与实际应用对应关系错误的是( )
| 选项 | 物质的性质 | 实际应用 |
| A | 二氧化锰具有强氧化性 | 用作H2O2分解的氧化剂 |
| B | 液氨汽化时要吸收大量的热 | 用作制冷剂 |
| C | Al2O3熔点高 | 用作耐高温材料 |
| D | 肥皂水显碱性 | 用作蚊虫叮咬处的清洗剂 |
| A. | A | B. | B | C. | C | D. | D |
6.钾是比钠活泼的金属,与水反应的产物与钠相似:2K+2H2O=2KOH+H2↑.将少量金属钾投入下列物质的水溶液中,有气体放出且溶液质量减轻的是( )
| A. | CuSO4 | B. | NaOH | C. | H2SO4 | D. | HC1 |
13.将10℃的0.2mol N2O4置于2L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g)?2NO2 (g).下列结论能说明上述反应在该条件下已经达到平衡状态的是( )
①烧瓶内气体的平均相对分子质量不再变化
②NO2的物质的量浓度不再改变
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤烧瓶内气体的颜色不再加深
⑥N2O4的消耗速率与NO2的生成速率之比为1:2
⑦NO2生成速率与NO2消耗速率相等
⑧烧瓶内气体的密度不再变化.
①烧瓶内气体的平均相对分子质量不再变化
②NO2的物质的量浓度不再改变
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤烧瓶内气体的颜色不再加深
⑥N2O4的消耗速率与NO2的生成速率之比为1:2
⑦NO2生成速率与NO2消耗速率相等
⑧烧瓶内气体的密度不再变化.
| A. | ①②③⑤⑦ | B. | ①②③⑤⑥⑦ | C. | ①②③④ | D. | ②③⑦⑧ |
10.不能用有关胶体的观点解释的现象是( )
| A. | 在江河入海处易形成三角洲 | |
| B. | AgNO3溶液中滴入同浓度NaCl溶液,生成白色沉淀 | |
| C. | 卤水点豆腐 | |
| D. | 同一钢笔同时使用不同牌号的墨水易发生堵塞 |
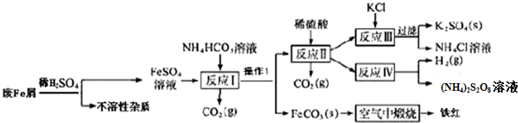
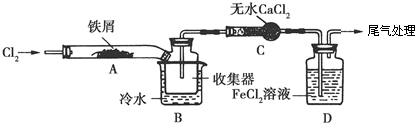
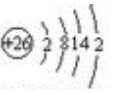 .FeCl3是共价化合物(填“离子”或“共价”).
.FeCl3是共价化合物(填“离子”或“共价”).