题目内容
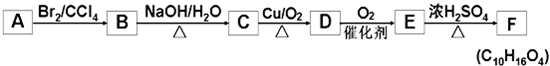
有机物A~E的转化关系如下所示.1molA能与1molBr2恰好完全反应;E的分子式为C5H10O3,1molE分别与Na、NaHCO3反应,消耗两者物质的量之比为2:1,氢核磁共振谱分析E有5组不同的特征峰.F分子结构中含有一个六元环.已知:
(1)E中含有的官能团名称是 ,E的结构简式是
(2)写出C→D的化学方程式 ,反应类型
(3)写出E→F的化学方程式 ,反应类型
(4)E转化为F过程中,可能发生多种副反应,写出含5个碳原子的副产物的键线式 、 .

(1)E中含有的官能团名称是
(2)写出C→D的化学方程式
(3)写出E→F的化学方程式
(4)E转化为F过程中,可能发生多种副反应,写出含5个碳原子的副产物的键线式
考点:有机物的推断
专题:有机物的化学性质及推断
分析:1molA能与1molBr2恰好完全反应,说明A中含有1个碳碳双键,A与溴发生加成反应生成B,B中含有溴原子,发生水解反应生成C,则C中含有2个羟基.C发生催化氧化生成D,则D中含有醛基.D继续被氧化生成E,则E中含有羧基.1molE分别与Na、NaHCO3反应,消耗两者物质的量之比为2:1,说明E中除了羧基,还含有1个羟基,说明与该羟基的相连的碳原子上没有氢原子.氢核磁共振谱分析E有5组不同的特征峰,所以E的结构简式为 ,逆推可知,D为
,逆推可知,D为 ,C为
,C为 ,B为
,B为 ,A为
,A为 .E在浓硫酸的作用下发生酯化反应生成F,F分子结构中含有一个六元环,则F的结构简式为
.E在浓硫酸的作用下发生酯化反应生成F,F分子结构中含有一个六元环,则F的结构简式为 .由于E中含有羟基,所以也可能发生消去反应生成碳碳双键,其结构简式为
.由于E中含有羟基,所以也可能发生消去反应生成碳碳双键,其结构简式为 或
或 .
.
 ,逆推可知,D为
,逆推可知,D为 ,C为
,C为 ,B为
,B为 ,A为
,A为 .E在浓硫酸的作用下发生酯化反应生成F,F分子结构中含有一个六元环,则F的结构简式为
.E在浓硫酸的作用下发生酯化反应生成F,F分子结构中含有一个六元环,则F的结构简式为 .由于E中含有羟基,所以也可能发生消去反应生成碳碳双键,其结构简式为
.由于E中含有羟基,所以也可能发生消去反应生成碳碳双键,其结构简式为 或
或 .
.解答:
解:1molA能与1molBr2恰好完全反应,说明A中含有1个碳碳双键,A与溴发生加成反应生成B,B中含有溴原子,发生水解反应生成C,则C中含有2个羟基.C发生催化氧化生成D,则D中含有醛基.D继续被氧化生成E,则E中含有羧基.1molE分别与Na、NaHCO3反应,消耗两者物质的量之比为2:1,说明E中除了羧基,还含有1个羟基,说明与该羟基的相连的碳原子上没有氢原子.氢核磁共振谱分析E有5组不同的特征峰,所以E的结构简式为 ,逆推可知,D为
,逆推可知,D为 ,C为
,C为 ,B为
,B为 ,A为
,A为 .E在浓硫酸的作用下发生酯化反应生成F,F分子结构中含有一个六元环,则F的结构简式为
.E在浓硫酸的作用下发生酯化反应生成F,F分子结构中含有一个六元环,则F的结构简式为 ,
,
(1)E为 ,含有的官能团是:羧基、羟基,故答案为:
,含有的官能团是:羧基、羟基,故答案为: ,羧基、羟基;
,羧基、羟基;
(2)C→D的化学方程式为2 +O2
+O2
2 +2H2O,属于氧化反应,
+2H2O,属于氧化反应,
故答案为:2 +O2
+O2
2 +2H2O,氧化反应;
+2H2O,氧化反应;
(3)E→F的化学方程式为2
 +2H2O,属于酯化反应,
+2H2O,属于酯化反应,
故答案为:2
 +2H2O,酯化反应;
+2H2O,酯化反应;
(4)由于E中含有羟基,所以也可能发生消去反应生成碳碳双键,其结构简式为 或
或 ,故答案为:
,故答案为: 或
或 .
.
 ,逆推可知,D为
,逆推可知,D为 ,C为
,C为 ,B为
,B为 ,A为
,A为 .E在浓硫酸的作用下发生酯化反应生成F,F分子结构中含有一个六元环,则F的结构简式为
.E在浓硫酸的作用下发生酯化反应生成F,F分子结构中含有一个六元环,则F的结构简式为 ,
,(1)E为
 ,含有的官能团是:羧基、羟基,故答案为:
,含有的官能团是:羧基、羟基,故答案为: ,羧基、羟基;
,羧基、羟基;(2)C→D的化学方程式为2
 +O2
+O2| 催化剂 |
 +2H2O,属于氧化反应,
+2H2O,属于氧化反应,故答案为:2
 +O2
+O2| 催化剂 |
 +2H2O,氧化反应;
+2H2O,氧化反应;(3)E→F的化学方程式为2

| 浓硫酸 |
| △ |
 +2H2O,属于酯化反应,
+2H2O,属于酯化反应,故答案为:2

| 浓硫酸 |
| △ |
 +2H2O,酯化反应;
+2H2O,酯化反应;(4)由于E中含有羟基,所以也可能发生消去反应生成碳碳双键,其结构简式为
 或
或 ,故答案为:
,故答案为: 或
或 .
.
点评:本题考查有机物推断,综合分析确定E的结构简式是关键,再利用逆推法推断,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列方程式中,属于水解反应的是( )
| A、H2O+H2O?H3O++OH- |
| B、HCO3-+H2O?H2CO3+OH- |
| C、HCO3-+H2O?H3O++CO32- |
| D、HCO3-+OH-?H2O+CO32- |
下列离子方程式正确的是( )
| A、FeI2溶液中滴入过量溴水 2Fe2++2I-+2Br2=2Fe3++I2+4Br- |
| B、Na2O2与H2O反应 2O22-+2H2O=4OH-+O2↑ |
| C、NaHSO4溶液中滴入少量Ba(OH)2 H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+=Cl2↑+H2O |
一定温度下,将0.1molAgCl加入1L 0.1mol?L-1Na2CO3溶液中,充分搅拌(不考虑液体体积变化),已知:Ksp(AgCl)=2×10-10;Ksp(Ag2CO3)=1×10-11,下列有关说法正确的是( )
| A、沉淀转化反应2AgCl(s)+CO32-(aq)?Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol?L-1 |
| B、约有2×10-5mol AgCl溶解 |
| C、反应后溶液中的:c(Na+)>c (Cl-)>c (CO32-)>c (OH-)>c (H+) |
| D、反应后溶液中的:c(Na+)+c (H+)+c (Ag+)=2 c (CO32-)+c (HCO3-)+c (Cl-)+c (OH-) |
已知反应①:CO(g)+CuO(s)?CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)?Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)?CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是( )
A、反应①的平衡常数K1=
| ||
B、反应③的平衡常数K=
| ||
| C、对于反应③,恒容时,温度升高,H2浓度减小,则该反应的△H>0 | ||
| D、对于反应③,恒温恒容下,增大压强,H2浓度一定减小 |
有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下,结论不正确的是( )
| 实验步骤 | 实验现象 |
| ①取少量该溶液,加几滴石蕊试剂 | 溶液变成红色 |
| ②取少量该溶液,加Cu片和浓H2SO4,加热 | 有无色气体产生,在空气中又变成红棕色 |
| ③取少量原溶液,加BaCl2溶液 | 有白色沉淀生成 |
| ④取③中上层清液,加AgNO3溶液 | 有白色沉淀生成,且不溶于稀HNO3 |
| ⑤取少量原溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH溶液过量时有部分沉淀溶解 |
| A、溶液中肯定不存在的离子是Fe2+、Ba2+、I-、HCO3- |
| B、溶液中肯定存在的离子是Al3+、NO3-、SO42-、Cl- |
| C、无法确定溶液中是否含有Na+、Cl- |
| D、要确定溶液中是否含Cl-,可取少量原溶液,加入足量Ba(NO3)2溶液后,取上层清液加入AgNO3溶液和稀HNO3 |
 使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.
使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.