题目内容
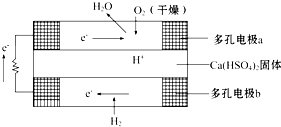 如图是某固体酸燃料电池基本结构示意图,其中以Ca(HSO4)2固体为电解质传递H+,电池总反应式为:2H2+O2═2H2O,下列有关说法不正确的是( )
如图是某固体酸燃料电池基本结构示意图,其中以Ca(HSO4)2固体为电解质传递H+,电池总反应式为:2H2+O2═2H2O,下列有关说法不正确的是( )| A、H2通过多孔电极时能增大H2的接触面积,加快反应 |
| B、a极上的电极反应式为:O2+2H2O+4e-═4OH- |
| C、每转移0.1 mol电子,消耗标准状况下的H2 1.12 L |
| D、H+由b极通过固体酸电解质传递到a极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据电池总反应:2H2+O2=2H2O可知:通入氢气的一极为电池的负极,发生氧化还原反应,反应为H2-2e-═2H+,通入氧气的一极为电池的正极,发生氧化反应,反应为O2+4e-+4H+=2H2O;电池工作时,电子通过外电路从负极流向正极,即从b极流向a极,电解质溶液中阳离子向正极移动,即H+由b极通过固体酸电解质传递到a极;每转移0.1mol电子,消耗0.05mol的H2,以此解答该题.
解答:
解:A.反应的接触面积越大,反应速率越大,故A正确;
B.该电池为酸性电池,所以正极电极反应为O2+4e-+4H+=2H2O,故B错误;
C.每转移0.1mol电子,消耗0.05mol的H2,标准状况下的H2 1.12 L,故C正确;
D.原电池中,阳离子向正极移动,所以H+由b极通过固体酸电解质传递到a极,故D正确.
故选B.
B.该电池为酸性电池,所以正极电极反应为O2+4e-+4H+=2H2O,故B错误;
C.每转移0.1mol电子,消耗0.05mol的H2,标准状况下的H2 1.12 L,故C正确;
D.原电池中,阳离子向正极移动,所以H+由b极通过固体酸电解质传递到a极,故D正确.
故选B.
点评:该题是高考中的常见题型,侧重考查学生灵活运用原电池原理解决实际问题的能力.学习中要明确原电池电子以及离子的定向移动问题,要能正确判断原电池的正负极,以及电极反应式的书写等问题,难度不大.

练习册系列答案
相关题目
 一定温度下,在2L的密闭容器中,A、B、C三种气体的物质的量随时间变化的曲线如图所示,下列叙述正确的是( )
一定温度下,在2L的密闭容器中,A、B、C三种气体的物质的量随时间变化的曲线如图所示,下列叙述正确的是( )| A、反应开始到2min,用A表示的反应速率为0.1 mol?Lˉ1?minˉ1 |
| B、反应开始到2min,B的物质的量浓度增加了0.2mol/L |
| C、反应进行到2min时,该反应停止了 |
| D、反应的化学方程式为:2A(g)?2B(g)+C(g) |
已知NaHSO3溶液显酸性,溶液中存在以下平衡:HSO3-+H2O?H2SO3+OH-①HSO3-?H++SO32-②,向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
| A、加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 | ||||||||
B、加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+
| ||||||||
C、加入少量NaOH溶液,
| ||||||||
| D、加入氨水至中性,则2c(Na+)=c(SO32-)>c(H+)=c(OH-) |
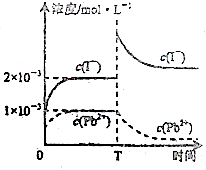 常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子浓度变化如图所示,下列有关说法正确的是( )
常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子浓度变化如图所示,下列有关说法正确的是( )| A、常温下,PbI2的Ksp为2×10-6 |
| B、温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度不变,Pb2+浓度不变 |
| C、常温下Ksp[PbS]=8×10-28,向PbI2的悬浊液中加入Na2S溶液,PbI2(s)+S2-(aq)?PbS(s)+2I-(aq)反应的化学平衡常数为5×1018 |
| D、T时刻改变的条件是由于升高温度,PbI2的Ksp增大 |
氢原子的3d和4s能级的能量高低是( )
| A、3d>4s |
| B、3d<4s |
| C、3d=4s |
| D、无3d、4s轨道,无所谓能量高低 |
下列有关能量转化的说法中正确的是( )
| A、铝热反应属于吸热反应 | ||||
| B、“H-CI→H+C1“过程中放出热量 | ||||
| C、干冰升华过程放出热量 | ||||
D、 反应“C+H2O
|


