题目内容
下列有关能量转化的说法中正确的是( )
| A、铝热反应属于吸热反应 | ||||
| B、“H-CI→H+C1“过程中放出热量 | ||||
| C、干冰升华过程放出热量 | ||||
D、 反应“C+H2O
|
考点:化学反应的能量变化规律,吸热反应和放热反应
专题:
分析:A.铝热反应会放出大量热;
B.断键吸收能量;
C.干冰升华吸收能量;
D.碳与水反应是吸热反应.
B.断键吸收能量;
C.干冰升华吸收能量;
D.碳与水反应是吸热反应.
解答:
解:A.铝热反应会放出大量热,即铝热反应属于放热反应,故A错误;
B.“H-CI→H+C1“断键吸收能量,故B错误;
C.干冰升华过程吸收能量,故C错误;
D.碳与水反应是吸热反应,生成物的总能量大于反应物的总能量,故D正确.
故选D.
B.“H-CI→H+C1“断键吸收能量,故B错误;
C.干冰升华过程吸收能量,故C错误;
D.碳与水反应是吸热反应,生成物的总能量大于反应物的总能量,故D正确.
故选D.
点评:本题考查化学反应的能量变化规律,难度不大,注意断键,物质由固态到气态吸收能量.

练习册系列答案
相关题目
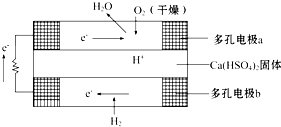 如图是某固体酸燃料电池基本结构示意图,其中以Ca(HSO4)2固体为电解质传递H+,电池总反应式为:2H2+O2═2H2O,下列有关说法不正确的是( )
如图是某固体酸燃料电池基本结构示意图,其中以Ca(HSO4)2固体为电解质传递H+,电池总反应式为:2H2+O2═2H2O,下列有关说法不正确的是( )| A、H2通过多孔电极时能增大H2的接触面积,加快反应 |
| B、a极上的电极反应式为:O2+2H2O+4e-═4OH- |
| C、每转移0.1 mol电子,消耗标准状况下的H2 1.12 L |
| D、H+由b极通过固体酸电解质传递到a极 |
短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍或者C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和.下列说法正确的是( )
| A、元素A所形成的氧化物只有一种 |
| B、元素B的最高价氧化物对应的水化物为强酸 |
| C、元素C、D、E的最高价氧化物对应的水化物两两之间可发生反应 |
| D、氢化物的稳定性:A>B |
下列叙述正确的是( )
| A、常温常压下,17g羟基中所含电子数为9NA |
| B、常温下,1 molFe与足量浓硝酸反应,转移2 NA个电子 |
| C、常温常压下,22.4L的NO2和CO2混合气体含有2 NA个O 原子 |
| D、在0.1 mol过氧化钠中,阴离子总数等于0.2 NA |
W、X、Y、Z均是短周期主族元素,X、Y、Z处于同一周期,W、X、Z的简单离子具有相同的电子层结构,W的最高价氧化物对应的水化物与其氢化物能反应生成盐,X的氧化物既能溶于酸又能溶于碱,Y的最高正价与最低负价的代数和为O.下列说法正确的是( )
| A、离子半径:W>X>Z |
| B、原子半径:Z>X>Y |
| C、单质的熔点:W>Z>Y |
| D、最高正价:Z>W>X |

