题目内容
14.下列关于铝及其化合物的叙述正确的是( )| A. | 氢氧化铝可作胃酸的中和剂 | B. | 工业上采用电解熔融氯化铝制铝 | ||
| C. | 铝罐可久盛食醋 | D. | 明矾用作净水剂不涉及化学变化 |
分析 A、氢氧化铝是弱碱;
B、工业上采用电解熔融氧化铝制铝;
C、铝罐可与食醋反应;
D、明矾在水中可以电离出两种金属离子K+、Al3+.而Al3+很容易水解,生成胶状的氢氧化铝,属于化学变化.
解答 解:A、氢氧化铝是弱碱,所以氢氧化铝可作胃酸的中和剂,故A正确;
B、工业上采用电解熔融氧化铝制铝,不是熔融氯化铝,故B错误;
C、铝罐可与食醋反应,所以不能用铝罐可久盛食醋,故C错误;
D、明矾在水中可以电离出两种金属离子K+、Al3+.而Al3+很容易水解,生成胶状的氢氧化铝,属于化学变化,氢氧化铝胶体的吸附能力很强,可以吸附水里悬浮的杂质,从而使杂质沉降水变澄清,属于物理变化,故D错误;
故选A.
点评 本题考查学生金属铝及其化合物的性质,难度不大.要注意化学变化和物理变化的本质区别是否有新物质生成.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
2.下列说法都正确的是( )
①生活中使用频率很高的一元纸币将逐步被硬币替代,硬币是合金
②江河入海口三角洲的形成通常与胶体的性质有关
③“钡餐”中使用的硫酸钡是弱电解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和H2O2,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物.
①生活中使用频率很高的一元纸币将逐步被硬币替代,硬币是合金
②江河入海口三角洲的形成通常与胶体的性质有关
③“钡餐”中使用的硫酸钡是弱电解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和H2O2,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物.
| A. | ①②③④ | B. | ①②④⑥ | C. | ①②⑤⑥ | D. | ③④⑤⑥ |
9.已知某反应是放热反应,下列说法正确的是( )
| A. | 该反应中反应物的总能量大于生成物的总能量 | |
| B. | 该反应中反应物的总能量小于生成物的总能量 | |
| C. | 该反应发生时,一定不需要加热 | |
| D. | 如果该反应开始后停止加热,反应一定能继续进行 |
19.下列关于价电子排布为3s23p4的原子描述正确的是( )
| A. | 它的元素符号为O | |
| B. | 它的核外电子排布式为1s22s22p63s23p4 | |
| C. | 可以与H2化合生成液态化合物 | |
| D. | 其电子排布图为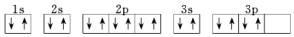 |
6.下列物质中,不能作为干燥剂的是( )
| A. | 蓝色硫酸铜 | B. | 液体浓硫酸 | C. | 无水氯化钙 | D. | 白色碱石灰 |
3.下列各组离子在溶液中能大量共存的是( )
| A. | Fe3+、Cl-、NO3- | B. | K+、HCO3-、OH- | C. | Na+、HCO3-、H+ | D. | NH4+、H+、SO32- |
16.构成金属晶体的基本微粒是( )
| A. | 分子 | B. | 原子 | ||
| C. | 阳离子与阴离子 | D. | 阳离子与自由电子 |
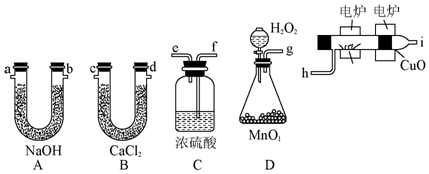
 ;
;