题目内容
10.下列说法正确的是( )| A. | 按系统命名法,有机物 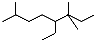 可命名为3,3,7-三甲基-4-乙基辛烷 可命名为3,3,7-三甲基-4-乙基辛烷 | |
| B. | 石油制乙烯、煤的液化、蛋白质的盐析、肥皂去油污均涉及化学变化 | |
| C. | 等质量的乙醇与乙烯完全燃烧,前者生成更多的水 | |
| D. | 全降解塑料 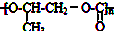 可由环氧丙烷( 可由环氧丙烷(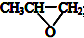 )和CO2反应制得 )和CO2反应制得 |
分析 A.主链含8个C,3、7号C上有甲基,4号C上有乙基;
B.蛋白质的盐析为物理变化;
C.等质量的乙醇与乙烯,含H质量分别为m×$\frac{6}{46}$、m×$\frac{4}{28}$;
D.全降解塑料(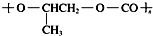 )可由单体环氧丙烷(
)可由单体环氧丙烷(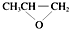 )和CO2加聚制得.
)和CO2加聚制得.
解答 解:A.主链含8个C,3、7号C上有甲基,4号C上有乙基,命名为3,3,7-三甲基-4-乙基辛烷,故A正确;
B.蛋白质的盐析为物理变化,而石油制乙烯、煤的液化、肥皂去油污均涉及化学变化,故B错误;
C.等质量的乙醇与乙烯,含H质量分别为m×$\frac{6}{46}$、m×$\frac{4}{28}$,后者生成水多,故C错误;
D.全降解塑料(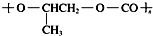 )可由单体环氧丙烷(
)可由单体环氧丙烷(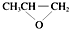 )和CO2加聚制得,发生加聚反应生成,故D正确;
)和CO2加聚制得,发生加聚反应生成,故D正确;
故选AD.
点评 本题考查有机物的结构与性质,为高频考点,把握物质的性质、发生的变化、有机物组成等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
1.化学与生产、生活密切相关.下列说法正确的是( )
| A. | 福尔马林可用于保存海鲜产品 | |
| B. | 硅胶吸附能力强,常用作催化剂载体和食品干燥剂 | |
| C. | 糖类、油脂、蛋白质在一定条件下都可以发生水解反应 | |
| D. | 明矾可以用于自来水的消毒 |
18.下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁的表面能形成致密的氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
| A. | A | B. | B | C. | C | D. | D |
5.下列反应属于氧化还原反应的是( )
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | Na2O+H2O═2NaOH | ||
| C. | 4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+O2↑+2H2O | D. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
2. 固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
其它传感器、探测器等方面的应用日益广泛.如RbAg4I5晶体,其中迁移的离子全是Ag+,固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
其它传感器、探测器等方面的应用日益广泛.如RbAg4I5晶体,其中迁移的离子全是Ag+,
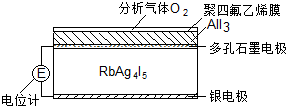
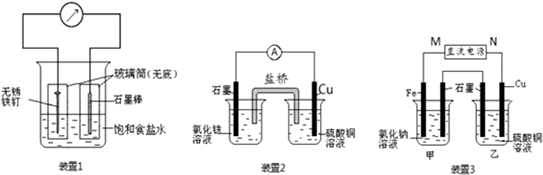
室温导电率达0.27Ω-1•cm-1.利用RbAg4I5晶体,可以制成电化学气敏传感器,下图是一种测定O2含量的气体传感器示意图.被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量.在气体传感器工作过程中,下列变化肯定没有发生的是( )
 固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及其它传感器、探测器等方面的应用日益广泛.如RbAg4I5晶体,其中迁移的离子全是Ag+,固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
其它传感器、探测器等方面的应用日益广泛.如RbAg4I5晶体,其中迁移的离子全是Ag+,
室温导电率达0.27Ω-1•cm-1.利用RbAg4I5晶体,可以制成电化学气敏传感器,下图是一种测定O2含量的气体传感器示意图.被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量.在气体传感器工作过程中,下列变化肯定没有发生的是( )
| A. | 4AlI3+3O2=2Al2O3+6I2 | B. | I2+2Ag++2e-=2AgI | ||
| C. | Ag-e-=Ag+ | D. | I2+2Rb++2e-=2RbI |
20.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,11.2LHCl和11.2LNH3充分混合后含有的分子数为NA | |
| B. | 0.1mol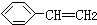 中含有碳碳双键的数目为0.4NA 中含有碳碳双键的数目为0.4NA | |
| C. | 常温常压下,1molNO2与水反应后,溶液中NO3-的数目为NA | |
| D. | 1molMg与足量空气反应生成MgO和Mg3N2,失去的电子数为2NA |
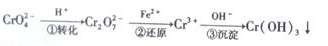
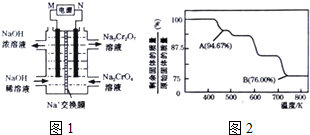
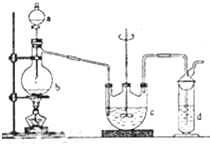 硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:
硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理: