题目内容
4.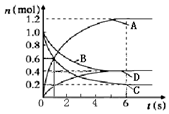 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应推断合理的是( )| A. | 该反应的化学方程式为3B+4C=6A+2D | |
| B. | 反应进行到1s时,3v(A)=v(D) | |
| C. | 反应进行到6s时,各物质的质量分数不变 | |
| D. | 反应进行到6s时,B的平均反应速率为0.1mol/(L•s) |
分析 由图可知,B、C的物质的量减小,A、D的物质的量增加,则B、C为反应物、A、D为生成物,B、C、A、D的△n之比为(1-0.4):(1-0.2):(1.2-0):(0.4-0)=1:2:3:1,6s时达到平衡,则反应为B+2C?3A+D,结合反应速率之比等于化学计量数之比、v=$\frac{△c}{△t}$计算.
解答 解:由图可知,B、C的物质的量减小,A、D的物质的量增加,则B、C为反应物、A、D为生成物,B、C、A、D的△n之比为(1-0.4):(1-0.2):(1.2-0):(0.4-0)=1:2:3:1,反应速率之比等于化学计量数之比,等于相同时间的物质的量变化量之比,6s时达到平衡,则反应为B+2C?3A+D,
A.由上述分析可知,反应为B+2C?3A+D,故A错误;
B.反应进行到1s时,v(A)=3v(D),故B错误;
C.反应进行到6s时,达到平衡,各物质的质量分数不变,故C正确;
D.反应进行到6s时,B的平均反应速率为$\frac{\frac{1.0mol-0.4mol}{2L}}{6s}$=0.05mol/(L•S),故D错误;
故选C.
点评 本题考查物质的量与时间的变化曲线,为高频考点,把握图中物质的量的变化、速率与化学计量数的关系为解答的关键,侧重分析与应用能力的考查,注意平衡状态的判断,题目难度不大.

练习册系列答案
相关题目
14.下列与化学概念有关的说法错误的是( )
| A. | 水在化学反应中既可做氧化剂又可做还原剂 | |
| B. | 14C和14N质量数相同,化学性质也相同 | |
| C. | 牛奶是一种胶体,能发生丁达尔现象 | |
| D. | “水滴石穿”是因为CaCO3与CO2、水发生了化学反应 |
9.如图为某反应的部分微观示意图,其中不同球代表不同元素的原子.下列说法正确的是( )
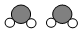 +
+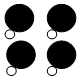 →
→ +4X.
+4X.
 +
+ →
→ +4X.
+4X.| A. | 该反应属于置换反应 | B. | 参加反应的两种分子个数比为1:1 | ||
| C. | 1个X分子中含有3个原子 | D. | 1个X分子中含有3种不同的原子 |
16.下列叙述中正确的是( )
| A. | 以Al作阳极,Fe作阴极,AlCl3溶液作电解液,可以实现铁上镀铝 | |
| B. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解 | |
| C. | 向纯水中加入盐酸或降温,都能使水的电离平衡逆向移动,水的离子积减小 | |
| D. | 同温同压下,反应H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
13.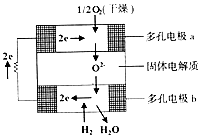 固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
 固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )| A. | O2-向电池的正极移动 | |
| B. | 有H2放电的b极为电池的正极 | |
| C. | a极对应的电极反应为O2+2H2O+4e-=4OH- | |
| D. | 该电池的总反应方程式为2H2+O2=2H2O |
14.下列说法正确的是( )
| A. | 锌锰电池和碱性锌锰电池的正极材料均是锌 | |
| B. | 锌锰电池中电解质主要是NH4Cl,而碱性锌锰电池中的电解质主要是KOH | |
| C. | 碱性锌锰电池不如锌锰电池的寿命长 | |
| D. | 干电池放电之后还可再充电 |
 电解饱和食盐水装置的结构如图所示:
电解饱和食盐水装置的结构如图所示: