题目内容
13.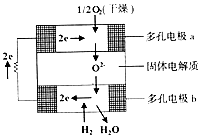 固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )| A. | O2-向电池的正极移动 | |
| B. | 有H2放电的b极为电池的正极 | |
| C. | a极对应的电极反应为O2+2H2O+4e-=4OH- | |
| D. | 该电池的总反应方程式为2H2+O2=2H2O |
分析 该电池属于固体燃料电池,以固体氧化锆-氧化钇为电解质,电池工作时,正极上氧气得电子生成阳离子,则正极上反应为O2+4e-=2O2-;负极为氢气失电子发生氧化反应,负极:2H2-4e-+2O2-═2H2O,总反应为:2H2+O2═2H2O.
解答 解:A.原电池工作时,阴离子移向负极,故A错误;
B.在燃料电池中,有H2参加的b极为原电池的负极,故B错误;
C.a极为正极,电解质不是溶液,所以电极反应为:O2+4e-=2O2-,故C错误;
D.该电池的总反应式为2H2+O2═2H2O,故D正确.
故选D.
点评 本题考查原电池的工作原理,涉及正负极的判断,电极反应式的书写等问题,题目难度不大,注意基础知识的积累.

练习册系列答案
相关题目
4.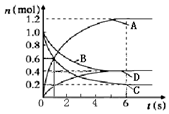 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应推断合理的是( )
 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应推断合理的是( )| A. | 该反应的化学方程式为3B+4C=6A+2D | |
| B. | 反应进行到1s时,3v(A)=v(D) | |
| C. | 反应进行到6s时,各物质的质量分数不变 | |
| D. | 反应进行到6s时,B的平均反应速率为0.1mol/(L•s) |
1.下列反应中,水只作氧化剂的是( )
| A. | Cl2+H2O═HCl+HClO | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | 2Na+2H2O═2NaOH+H2↑ | D. | 2H2O $\frac{\underline{\;电解\;}}{\;}$ 2H2↑+O2↑ |
8.常温下,在无色透明的酸性溶液中一定能大量共存的离子组是( )
| A. | Na+、NH4+、SO42-、NO3- | B. | Na+、K+、SO42-、Cu2+ | ||
| C. | Ca2+、K+、Cl-、CO32- | D. | Mg2+、Fe3+、OH-、Cl- |
18.下列有关化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+(2×283.0)kJ/mol | |
| C. | 甲烷的燃烧热△H=-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| D. | Mg在CO2中燃烧生成MgO和C,该反应中化学能全部转化为热能 |
5.用如图所示装置进行如下实验,不能达到实验目的是( )
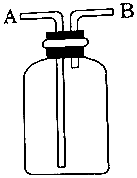

| A. | A瓶中盛满水,从B口进气,用排水法收集O2 | |
| B. | 瓶中盛适量浓硫酸,从A口进气来干燥Cl2 | |
| C. | 从B口进气,用排空气法收集Cl2 | |
| D. | 瓶中装满水,A口连导管并伸入量筒中,从B口进气,用排水法测量生成H2的大约体积 |
2.对下列实验过程的评价,正确的是( )
| A. | 某固体中加入稀盐酸,产生了无色气体,证明该固体一定会有CO32- | |
| B. | 某溶液中滴加了Na2CO3溶液,生成白色沉淀,该溶液中一定会有Ba2+ | |
| C. | 某无色溶液滴加酚酞试液显红色,该溶液不一定是碱液 | |
| D. | 验证烧碱溶液中是否含Cl-,先加稀HCl除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl- |
9.1918年,德国化学家弗里茨•哈伯因为发明合成氨方法而获得诺贝尔化学奖.1931年,卡尔•博施因为改进合成氨方法获得诺贝尔化学奖.2007年10月诺贝尔化学奖授予了德国化学家格哈德•埃特尔,理由是他发现了哈伯一博施法合成氨的作用机理.现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生,下列有关说法正确的是( )
| A. | 达到化学平衡时,将完全转化为NH3 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 | |
| C. | 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | |
| D. | 达到化学平衡时,正反应速率和逆反应速率都为零 |
 ,还可以写成
,还可以写成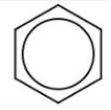 ,1mol苯可以跟3molH2发生加成反应生成环己烷,环己烷的结构简式为
,1mol苯可以跟3molH2发生加成反应生成环己烷,环己烷的结构简式为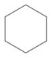 .
.