题目内容
7.下列反应能使溶液导电性显著减弱的是( )| A. | NaCl溶液中滴加AgNO3溶液 | B. | Na2CO3溶液中滴加盐酸 | ||
| C. | CH3COOH溶液中滴加氨水 | D. | CuSO4溶液中滴加Ba(OH)2溶液 |
分析 电解质溶液导电性与离子浓度成正比,与电荷成正比,反应后能使溶液导电性显著减弱,说明反应前后离子浓度减小变化较明显,据此分析解答.
解答 解:A.二者反应生成硝酸钠和AgCl沉淀,离子浓度变化不大明显,则溶液导电性变化不明显,故A不选;
B.碳酸钠和稀盐酸反应生成碳酸氢钠、氯化钠,继续滴加稀盐酸,碳酸氢钠和稀盐酸反应生成氯化钠、二氧化碳和水,离子浓度变化不明显,则溶液导电性变化不明显,故B不选;
C.醋酸是弱电解质,醋酸溶液中离子浓度较小,加入氨水后二者反应生成强电解质醋酸氨,离子浓度变化明显,溶液导电性显著增强,故C不选;
D.硫酸铜和氢氧化钡反应生成沉淀硫酸钡和沉淀氢氧化铜,当二者恰好完全反应时溶液中离子浓度接近0,溶液导电性变化明显减弱,故D选;
故选D.
点评 本题考查离子反应及溶液导电性,为高频考点,明确溶液导电性强弱影响因素是解本题关键,注意:溶液导电性强弱与电解质强弱、电解质溶解性强弱都无关,只与电解质溶液中离子浓度、离子所带电荷有关,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列指定反应的离子方程式正确的是( )
| A. | Cu 溶于稀 HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| B. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 用CH3COOH溶解 CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | FeCl3溶液与Cu反应:2Fe3++Cu═2Fe2++Cu2+ |
18.NA表示阿伏加德罗常数的值,下列说法一定正确的是( )
| A. | 标准状况下,12g石墨中含有2NA个C-C键 | |
| B. | 室温下,22.4L正戊烷中含有16NA个σ键 | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA | |
| D. | 62g P4分子中含有2NA个P-P键 |
15.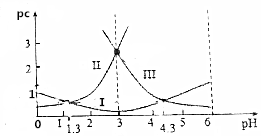 草酸(H2C2O4)水溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)随着溶液pH的变化曲线如图所示,下列说法中不正确的是( )
草酸(H2C2O4)水溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)随着溶液pH的变化曲线如图所示,下列说法中不正确的是( )
 草酸(H2C2O4)水溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)随着溶液pH的变化曲线如图所示,下列说法中不正确的是( )
草酸(H2C2O4)水溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)随着溶液pH的变化曲线如图所示,下列说法中不正确的是( )| A. | pH=4时,c(HC2O4-)>c(C2O42-) | |
| B. | c(H2C2O4)+c(HC2O4-)+c(C2O42-)一定不变 | |
| C. | 草酸的电离常数Ka1=10-1.3 | |
| D. | $\frac{c({C}_{2}{{O}_{4}}^{2-})•c({H}_{2}{C}_{2}{O}_{4})}{{c}^{2}(H{C}_{2}{{O}_{4}}^{-})}$=10-3 |
12.下列说法中正确的是( )
| A. | 在化合物CaCl2中,除了有Ca2+与Cl-之间的离子键外,还有两个Cl-之间的共价键 | |
| B. | 碘受热升华时共价键被破坏 | |
| C. | 熔化状态下能导电的化合物中一定存在离子键 | |
| D. | 离子化合物中可能含有共价键,共价化合物中可能含有离子键 |
19.硫酸铵溶液中离子浓度关系不正确的是( )
| A. | c(NH4+)>c(SO42-)>c(H+)>c(OH-) | B. | c(NH4+)=2c(SO42-) | ||
| C. | c(NH4+)+c(NH3•H2O)=2c(SO42-) | D. | c(NH4+)+c(H+)=c(OH-)+2c(SO42-) |
16.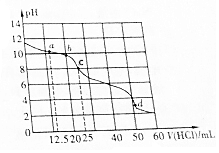 常温下,在VmL0.01mol•L-1的BOH溶液中滴加0.01mol•L-1盐酸,溶液pH与盐酸体积之间的关系如图所示.下列推断不正确的是( )
常温下,在VmL0.01mol•L-1的BOH溶液中滴加0.01mol•L-1盐酸,溶液pH与盐酸体积之间的关系如图所示.下列推断不正确的是( )
 常温下,在VmL0.01mol•L-1的BOH溶液中滴加0.01mol•L-1盐酸,溶液pH与盐酸体积之间的关系如图所示.下列推断不正确的是( )
常温下,在VmL0.01mol•L-1的BOH溶液中滴加0.01mol•L-1盐酸,溶液pH与盐酸体积之间的关系如图所示.下列推断不正确的是( )| A. | BOH电离方程式为BOH═B++OH- | |
| B. | 该盐酸溶液的pH=2 | |
| C. | 点c表示的溶液中c(OH-)=1.0×10-6mol•L-1 | |
| D. | BOH(aq)+HCl(aq)═BCl(aq)+H2O(l)△H<0 |
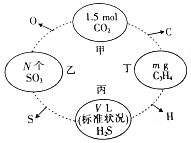 如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)
如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)