��Ŀ����
2��Na2S��H2O2�ڴӺ�����Ʒ������������⣬������CuZnFeCr�����ʣ�����ȡ����������ʱ����Ҫ���ã���ȡ�������£��ٵ�Ʒ������ù���������ữ�������õ���Һ��
������Һ�е���������Na2S��Һ����ȥCu2+ Zn2+��
�۱�����Һ��40�����ң���6%��H2O2��Һ����Fe2+������95��ʱ����NaOH��Һ���� pH�����˳�ȥ������
������Һ�м�������Na2CO3��Һ�����裬��NiCO3������
�ݡ�
��1��������г��ɹ۲쵽��ɫ�����⣬�����ᵽ��������ζ�������ӷ���ʽ˵������IJ�����S2-+2H+=H2S��
��2�����������Fe2+ �����Σ���Ҫ�����¶Ȳ�����40�棬��Ŀ���Ǽ��ٹ�������ķֽ⣻�ýη�����Ӧ�����ӷ���ʽΪ2Fe2++H2O2+2H+=2Fe3++2H2O��
��3��Fe2+ Ҳ������NaClO3������Fe2+���������ڽ�СpH������ˮ�⣬�����γɻ������Ƴ���������ȥ����֪25��ʱ��Fe��OH��3��Ksp=2.64��10 -39]������˵����ȷ����C������ĸ����
a��FeOOH����Ϊ+2��
b������25��ʱ����H2O2����Fe2+������pH=4ʱ��ȥ������ʱ��Һ��c��Fe3+ ��=2.64��10 -29 mol•L-1
c��������������������������Fe2+ �����ӷ���ʽΪ6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O
��4����ˮNiCl2���л��ϳ������ż�Ϊ��Ҫ�����ã���ҵ�ϳ��ú���ԭ�����Ƶõ�NiCl2•6H2O���������ȣ�SOCl2���м�����ˮ�Ƶã���֪SOCl2����ˮ��Ӧ����SO2��HCl��д��NiCl2•6H2O���������ȣ�SOCl2���м�����ˮ����ˮNiCl2�ķ�Ӧ����ʽNiCl2•6H2O+6SOCl2$\frac{\underline{\;\;��\;\;}}{\;}$NiCl2+6SO2+12HCl��NiCl2•6H2O�����������ȣ�SOCl2���м�����ˮ��ԭ����NiCl2�ڼ��ȹ����лᷢ��ˮ����ò�����ˮNiCl2����NiCl2•6H2O���������ȣ�SOCl2���м�����ˮʱ����Ӧ�����в�����HCl������NiCl2��ˮ�⣮
���� ��1��ԭ��Һ�ữ���������ӣ�����2�м������ƺ��г�������ζ���������ɣ�����ΪH2S��
��2�������¶�40�棬�������������ӵ�ͬʱ��ֹ˫��ˮ�ֽ⣮˫��ˮ�����������ӣ�
��3��A�����ݻ��������ữ�ϼ۴�����Ϊ0���㣻
B��pH=4ʱ������������Ũ��Ϊ10-10mol/L������Fe��OH��3��Ksp=2.64��10 -39]������õ�Fe3+��Ũ�ȣ�
C��������������������������Fe2+ ��Ϊ�����ӣ���������ԭΪ�Ȼ��ƣ����ԭ���غ�͵���غ������
��4������������ˮ�ܷ�Ӧ���ɶ���������Ȼ��⣬�ʿ�������Ni2+ˮ�⣬����������ˮ�ܷ�Ӧ���ɵ��Ȼ���Ҳ������Ni2+ˮ�⣮
��� �⣺��1��ԭ��Һ�ữ���������ӣ�����2�м������ƺ��г�������ζ���������ɣ�����ΪH2S����Ӧ�����ӷ���ʽΪ��S2-+2H +=H2S����
�ʴ�Ϊ��S2-+2H +=H2S����
��2����Ҫ�����¶Ȳ�����40�棬��Ŀ�����������������ӵ�ͬʱ��ֹ˫��ˮ�ֽ⣮˫��ˮ�����������ӵķ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O��
�ʴ�Ϊ�����ٹ�������ķֽ⣻2Fe2++H2O2+2H+=2Fe3++2H2O��
��3��A�����ݻ��������ữ�ϼ۴�����Ϊ0���㣬FeOOH��Fe�Ļ��ϼ�Ϊ+3����A����
B����pH=4ʱ������������Ũ��Ϊ10-10mol/L������Fe��OH��3��Ksp=2.64��10 -39]������õ�Fe3+��Ũ��=$\frac{Ksp}{{c}^{3}��O{H}^{-}��}$=$\frac{2.64��1{0}^{-39}}{��1{0}^{-10}��^{3}}$=2.64��10-9mol/L����B����
C������������������������Fe2+ ��Ϊ�����ӣ���������ԭΪ�Ȼ��ƣ����ԭ���غ�͵���غ���д�õ����ӷ���ʽΪ�����ӷ���ʽΪ6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O����C��ȷ��
�ʴ�Ϊ��C��
��4������������NiCl2•6H2O�����ڼ��ȹ�����NiCl2�ᷢ��ˮ����ò�����ˮNiCl2����NiCl2•6H2O���������ȣ�SOCl2���м�����ˮʱ����Ӧ�����в�����HCl������NiCl2��ˮ�⣬����������ˮ�ܷ�Ӧ���ɶ���������Ȼ��⣬�ʿ�������Ni2+ˮ�⣬NiCl2•6H2O���������ȣ�SOCl2���м�����ˮ����ˮNiCl2�ķ�Ӧ����ʽΪ��NiCl2•6H2O+6SOCl2$\frac{\underline{\;\;��\;\;}}{\;}$NiCl2+6SO2+12HCl��
�ʴ�Ϊ��NiCl2•6H2O+6SOCl2$\frac{\underline{\;\;��\;\;}}{\;}$NiCl2+6SO2+12HCl��NiCl 2�ڼ��ȹ����лᷢ��ˮ����ò�����ˮNiCl2����NiCl 2•6H2O���������ȣ�SOCl2���м�����ˮʱ����Ӧ�����в�����HCl������NiCl2��ˮ�⣮
���� ���⿼�����ʷ�����ᴿ�ķ��������̷����жϣ����ӷ���ʽ�ͻ�ѧ����ʽ��д����Ҫ��ʵ����ƺ��������ʵ�����Ӧ�ã����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�| A�� | Ҫ���鼺ϩ���Ƿ���������ױ���Ӧ�ȼ�������ˮ��Ȼ���ټ������Ը��������Һ | |
| B�� | ����Ũ�����Ũ����Ļ���ʱ����Ũ�����رڻ������뵽Ũ������ | |
| C�� | ��������ʱ����ʢ�л��Һ���Թ�ֱ���ھƾ��ƻ����ϼ��� | |
| D�� | ��ȥ�������������������ᣬ���Լ�����������Һ���Һ |
| A�� | ����Ͷ�뵽��Ũ�����У�2Al+6H+=2Al3++3H2�� | |
| B�� | �������ᷴӦ��2Fe+6H+=2Fe3++3H2�� | |
| C�� | ��С�մ�����θ����ࣺH++HCO3-=H2O+CO2�� | |
| D�� | Ba��OH��2��ϡH2SO4��Ӧ��Ba2++OH-+H++SO42-=BaSO4��+H2O |
| A�� | 1��1 | B�� | 2��1 | C�� | 1��2 | D�� | 2��3 |
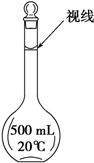 ʵ��������500mL 0.2mol/L��FeSO4��Һ��ʵ����������У�
ʵ��������500mL 0.2mol/L��FeSO4��Һ��ʵ����������У�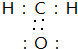
 ��M�������ӵ����ӷ���ΪO22-��
��M�������ӵ����ӷ���ΪO22-��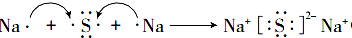 ��
��
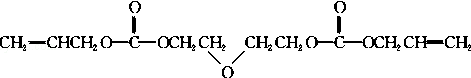
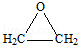 ��
��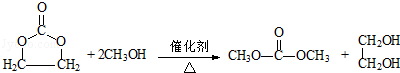 ��
��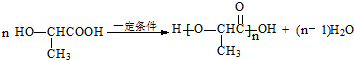 ��
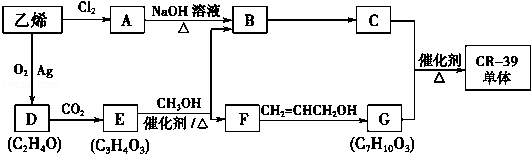
��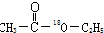 �ĺϳ�·�ߣ��ϳ�·������ͼʾ�����£�CH2-CH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH��
�ĺϳ�·�ߣ��ϳ�·������ͼʾ�����£�CH2-CH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH�� ��
��