题目内容
13.锂和镁在元素周期表中有特殊的“对角关系”,它们的单质及其化合物性质相似,下列关于锂及其化合物的叙述中可能正确的是( )| A. | Li2SO4难溶于水 | B. | LiOH加热时,不会分解 | ||
| C. | Li遇浓H2SO4发生钝化 | D. | Li2CO3加热时,分解成Li2O和CO2 |
分析 根据金属镁和化合物的性质知识来确定金属锂以及其化合物的性质.
解答 解:A、硫酸镁易溶于水,所以硫酸锂是易溶于水的,故A错误;
B、氢氧化镁是难溶于水,受热易分解的强碱,所以LiOH应该是难溶于水,受热分解的强碱,故B错误;
C、金属镁与浓硫酸不发生钝化现象,所以锂遇浓硫酸不发生钝化,故C错误;
D、碳酸镁受热分解生成氧化镁和二氧化碳,所以推知碳酸锂受热分解,生成Li2O和CO2,故D正确.
故选D.
点评 本题考查学生元素周期律的应用知识,侧重于考查学生对基础知识的综合应用的能力和知识的迁移能力,题目难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
17. (1)基态Cl原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(1)基态Cl原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(2)金属锂氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+<H-(填“>”、“=”或“<”).
②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
M是Mg(填元素符号).
(3)Cu2+基态的电子排布式为1s22s22p63s23p63d9sp3;向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4•H2O晶体,硫酸根离子中硫原子的杂化方式为sp3;不考虑空间构型,其内界结构可用示意图表示为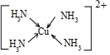 .
.
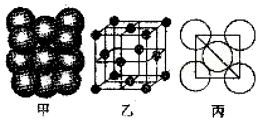
(4)某单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示,若已知该原子半径为d,NA表示阿伏伽德罗常数.摩尔质量为M,则该原子的配位数为12,该晶体的密度可表示为$\frac{{M}_{r}}{4\sqrt{2}(d×1{0}^{-10})^{3}{N}_{A}}$.
 (1)基态Cl原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(1)基态Cl原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.(2)金属锂氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+<H-(填“>”、“=”或“<”).
②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)Cu2+基态的电子排布式为1s22s22p63s23p63d9sp3;向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4•H2O晶体,硫酸根离子中硫原子的杂化方式为sp3;不考虑空间构型,其内界结构可用示意图表示为
 .
.(4)某单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示,若已知该原子半径为d,NA表示阿伏伽德罗常数.摩尔质量为M,则该原子的配位数为12,该晶体的密度可表示为$\frac{{M}_{r}}{4\sqrt{2}(d×1{0}^{-10})^{3}{N}_{A}}$.
4.下列能使淀粉溶液变蓝的物质是( )
| A. | KI | B. | KIO3 | C. | I2 | D. | KIO |
1.有关反应原理说法错误的是( )
| A. | 碳酸钙与盐酸反应过程中,再增加CaCO3固体的量,反应速率不变,但把CaCO3固体粉碎,可以加快反应速率 | |
| B. | 增大反应体系的压强,反应速率不一定增大 | |
| C. | 由温度或压强改变引起的平衡正向移动,反应物的转化率一定增大 | |
| D. | 对于2SO2(g)+O2(g)?2SO3(g)反应,当密度保持不变,在恒温恒容或恒温恒压条件下,均不能作为达到化学平衡状态的标志 |
8.在NaCl和Na2SO4的混合溶液中,Na+、SO42-、Cl-的物质的量浓度之比不可能出现的是( )
| A. | 8:3:2 | B. | 6:2:3 | C. | 5:2:1 | D. | 3:1:1 |
18.下列实验装置错误的是( )
| A. | 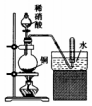 实验室制备NO | B. |  实验室制取NH3 | ||
| C. | 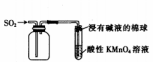 收集SO2并验证其还原性 | D. |  验证铜绿受热分解的酸性气体产物 |
2.下列关于电解质的判断中,正确的观点是( )
| A. | 在熔融状态下能导电的物质 | |
| B. | 在水溶液或熔融状态下能导电的物质 | |
| C. | 在水溶液或熔融状态下能导电的化合物 | |
| D. | 在水溶液和熔融状态下都能导电的化合物 |
3.下列有关实验操作、现象和目的或结论的说法正确的是( )
| 选项 | 操作 | 目的或结论 |
| A | 将Fe(NO3)2晶体溶于稀硫酸后,滴加KSCN溶液,观察溶液是否变化 | 检验Fe(NO3)2样品是否已被氧化而变质 |
| B | 海带提碘实验中,为了制取海带灰的浸取液,需要煮沸海带灰和水的混合物1-2min | 主要目的是去除溶液中的氧气,避免氧气氧化碘离子 |
| C | 在试管中依次加入2mL浓硫酸、3mL乙醇和2mL乙酸,用酒精灯缓慢加热 | 制备乙酸乙酯 |
| D | 向盛有少量Mg(OH)2固体的试管中加入适量NH4Cl浓溶液,充分震荡,白色固体溶解 | NH4+与Mg(OH)2溶解出的OH-结合,导致Mg(OH)2溶解 |
| A. | A | B. | B | C. | C | D. | D |